
科目: 来源: 题型:
【题目】氨是动植物生长不可缺少的元素,氨在自然界中的循环对生命有重要意义。其循环示意图如下:
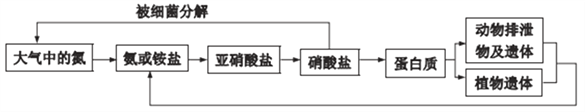
(1) 氨分子的电子式是__________。
(2) NH3是重要的化工原料,用途广泛,如合成尿素等。合成尿素原理分两步:
CO2(g)+ 2NH3(g)=NH2COONH4(s) △H1=- 159.5kJ/mol
NH2COONH4(s) = CO(NH2)2(s) + H2O(g) △H2=+28.5kJ/mol
则2NH3(g)+ CO2(g)=CO(NH2)2(s) + H2O(g) △H=_______kJ/mol
(3) 氯化铵也是氨的重要化合物,现有25℃时某浓度的氯化铵溶液中NH3·H2O和NH4+的浓度随pH的变化示意图如图I所示,则图中曲线①代表的是__________[填c(NH3·H2O)或c(NH4+)]该温度下NH3·H2O 电离平衡常数为___________(用a 的代数式表示)。
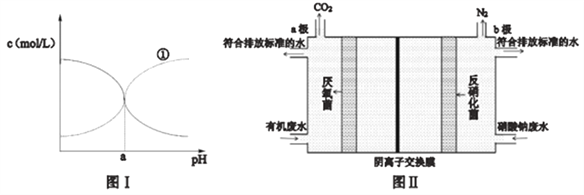
(4) 在厌氧环境下,土壤中的某些微生物(细菌)可将硝酸盐还原成氮气而实现自然界中的氮循环。某研究性学习小组由“自然界中的氮循环”产生联想:利用微生物的作用将化学能转化为电能即设计成微生物电池来同时处理含硝酸钠和有机物的废水,装置原理如图II(图中有机物用C6H12O6表示).写出电极b上的电极反应式__________________。
(5) 将游离态的氮转化为化合态的氮叫做氮的固定,其中一种重要的人工固氮就是合成氨。现维持温度为T压强为P的条件下,向一容积可变的密闭容器中通入1molN2和3molH2发生N2(g) +3H2(g)![]() 2NH3(g)的反应。容器容积与反应时间的数据关系如下表:
2NH3(g)的反应。容器容积与反应时间的数据关系如下表:
时间/min | 0 | 5 | 10 | 20 | 40 | 80 |
容器 容积/L | 4.00V | 3.20V | 2.80V | 2.60V | 2.50V | 2.50V |
该条件下达平衡时H2的转化率α(H2)=______,平衡常数K=_________(用V表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中不正确的是
A. ![]() 和
和 ![]() 是同一种核素
是同一种核素
B. 红磷和白磷互为同素异形体
C. CH3COOCH2CH3和CH3CH2COOCH3是不同种物质
D. CH3CH2OH可看做是由乙基和羟基两种基团组成的
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.某温度(t℃)时,水的Kw=10-13,则该温度(填 “大于”“小于”或“等于”)_________ 25℃,理由是_________,将此温度下pH =11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
(1)若所得混合液为中性,则a∶b_________;
(2)若所得混合液的pH=2,则a∶b_________。
Ⅱ.25℃时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,下列说法不正确的是(_____)
A.该溶液pH=4 B.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
C.此酸的电离平衡常数约为1×10-7 D.升高温度,溶液的pH增大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关石墨晶体的说法正确的是( )
A. 由于石墨晶体导电,所以它是金属晶体
B. 由于石墨的熔点很高,所以它是原子晶体
C. 由于石墨质软,所以它是分子晶体
D. 石墨晶体是一种混合晶体
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A. 加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)不变
B. 加入水稀释时,平衡向正反应方向移动,溶液中所有离子的浓度都减小
C. 加入少量CH3COONa固体,平衡向逆反应方向移动,平衡常数变大
D. 加入少量NaOH固体,促进了醋酸的电离,溶液中![]() 变大
变大
查看答案和解析>>
科目: 来源: 题型:
【题目】钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:
![]()
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)2·4H2O;
②25℃时,BaCO3的溶度积Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合价为:__________。
(2)用盐酸酸浸时发生反应的离子方程式为: __________。
(3)流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有_____________________。
②如何证明晶体已洗净?_______________________。
(4)TiO2具有很好的散射性,是一种有重要用途的金属氧化物。工业上可用TiCl4水解来制备,制备时需加入大量的水,同时加热,其目的是:_______________。
(5)某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3,得产品13.98g,BaTiO3的产率为:________。
(6)流程中用盐酸酸浸,其实质是BaCO3溶解平衡的移动。若浸出液中c(Ba2+)=0.1mol/L,则c(CO32-)在浸出液中的最大浓度为__________ mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】有下列六种物质的溶液:①NaCl ②NH4Cl ③Na2CO3 ④Al2(SO4)3 ⑤CH3COOH ⑥NaHCO3。
(1)25℃时,0.1mol·L-1②溶液的pH________7(填“>”、“=”或“<”);其原因是______________________________________(用离子方程式表示);
(2)常温下,浓度均为0.1mol/L的③和⑥的溶液中离子种类________(填“相同”或是“不相同”);
(3)将④溶液加热蒸干并灼烧最终得到的物质是____________(填化学式);
(4)常温下0.1 mol/L的⑤溶液加水稀释过程中,下列表达式的数据一定变大的是_________。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】按下列四种有关性质的叙述,可能属于金属晶体的是( )
A. 由分子间作用力结合而成,熔点低
B. 固体或熔融后易导电,熔点在1000 ℃左右
C. 由共价键结合成网状结构,熔点高
D. 固体和熔融状态不导电,但溶于水后可能导电
查看答案和解析>>
科目: 来源: 题型:
【题目】关于晶体的下列说法正确的是( )
A. 在晶体中只要有阴离子就一定有阳离子
B. 在晶体中只要有阳离子就一定有阴离子
C. 原子晶体的熔点一定比金属晶体的高
D. 分子晶体的熔点一定比金属晶体的低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com