
科目: 来源: 题型:
【题目】以石油裂解气为原料,通过一系列化学反应可得到重要的化工产品增塑剂G。流程如图所示
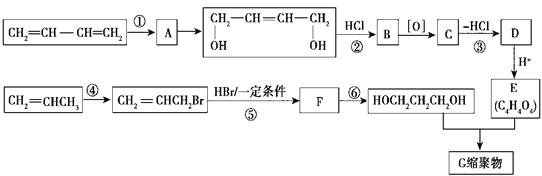
请完成下列各题:
(1)反应①发生的反应类型是 _________________。
(2)反应③发生的反应条件是 __________________。
(3)反应②、③的目的是 ________________________________________。
(4)写出反应⑤的化学方程式 ____________________________________________。
(5) B被氧化成C的过程中会有中间产物生成,该中间产物可能是 __________________(写出一种物质的结构简式),检验该物质存在的试剂是 _________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

请回答下列问题:
(1)环戊二烯分子中最多有 __________个原子共平面;
(2)金刚烷的分子式为 ____________ ;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:

其中,反应①的产物名称是 __________,反应②的反应试剂和反应条件是 __________。
(4)已知烯烃能发生如下反应:

请写出下列反应产物的结构简式:
![]()
![]() ____________________________________。
____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应H2(g) + I2(g) ![]() 2HI(g)达到平衡的标志是 ( )
2HI(g)达到平衡的标志是 ( )
A. H2、I2、HI的浓度相等 B. H2、I2、HI的浓度保持不变
C. 混合气体的密度保持不变 D. 混合气体的体积保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图,下列说法正确的是( )

A. M的最高价氧化物对应水化物能分别与Z、R的最高价氧化物对应水化物反应
B. Y的单质能从含R简单离子的水溶液人中置换出R单质
C. X、N两种元素组成的化合物熔点很低
D. 简单离子的半径:Z<X< Y
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式碳酸铜和氯气都是用途广泛的化工原料。
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H+、Cl)制备碱式碳酸铜,其制备过程如下:
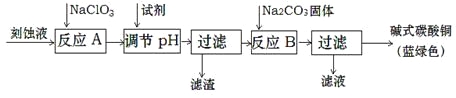
已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
开始沉淀pH | 4.2 | 5.8 | 1.2 |
完全沉淀pH | 6.7 | 8.3 | 3.2 |
①氯酸钠的作用是 ;
②反应A后调节溶液的pH范围应为 。
③第一次过滤得到的产品洗涤时,如何判断已经洗净? 。
④造成蓝绿色产品中混有CuO杂质的原因是 。
(2)某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。

①实验室用二氧化锰和浓盐酸加热制取氯气,所用仪器需要检漏的有 。
②若C中品红溶液褪色,能否证明氯气与水反应的产物有漂白性,说明原因 。此时B装置中发生反应的离子方程式是___________ _____。
③写出A溶液中具有强氧化性微粒的化学式 。若向A溶液中加入NaHCO3粉末,会观察到的现象是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇分子中不同的化学键如图,关于乙醇在各种反应中断裂键的说法不正确的是( )

A. 乙醇和钠反应,键①断裂
B. 在Ag催化下和O2反应,键①③断裂
C. 乙醇和浓H2SO4共热140℃时,键①或键②断裂;在170℃时,键②⑤断裂
D. 乙醇完全燃烧时断裂键①②
查看答案和解析>>
科目: 来源: 题型:
【题目】反应N2O4(g)![]() 2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )

A. a、c两点的反应速率:a>c
B. a、c两点气体的颜色:a深,c浅
C. b、c两点的转化率:b>c
D. 由b点到a点,可以用加热的方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com