
科目: 来源: 题型:
【题目】下列各组物质发生状态变化时,所克服的微粒间的相互作用,属于同种类型的是( )
A. 金刚石和硫的熔化 B. 食盐和石蜡的熔化
C. 碘和干冰的升华 D. 二氧化硅和氧化钠的熔化
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机物的叙述正确的是( )
A. 乙烯、聚乙烯均能使溴水褪色
B.  和
和 互为同分异构体
互为同分异构体
C. 苯在催化剂作用下能与浓硝酸发生取代反应
D. 等质量的甲烷和乙烯完全燃烧,乙烯消耗的O2多![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列表示资源开发、回收、利用原理的反应方程式不正确的是( )
A. 海水提溴时用SO2吸收Br2蒸气:SO2+Br2+2H2O=2HBr+H2SO4
B. 将煤气化为可燃性气体:C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
C. 用过量NaOH溶液吸收烟气中的SO2:SO2+NaOH=NaHSO3
D. 可以用铝和氧化铁制备铁单质:2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
查看答案和解析>>
科目: 来源: 题型:
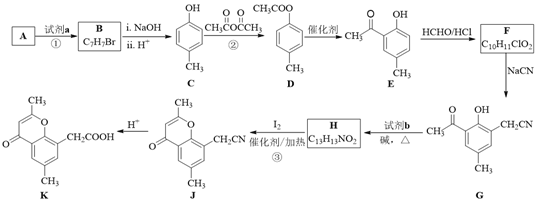
【题目】具有抗菌、消炎作用的黄酮醋酸类化合物L的合成路线如下图所示:
已知部分有机化合物转化的反应式如下:
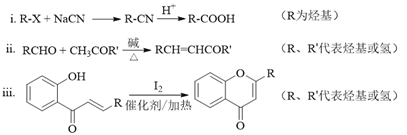
(1)A的分子式是C7H8,其结构简式是______;A→B所属的反应类型为______。
(2)C→D的化学方程式是______。
(3)写出满足下列条件的D的任意一种同分异构体的结构简式:______。
a.能发生银镜反应
b.分子中含有酯基
c. 苯环上有两个取代基,且苯环上的一氯代物有两种
(4)F的结构简式是______;试剂b是______。
(5)H与I2反应生成J和HI的化学方程式是______。
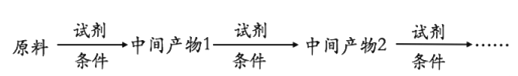
(6)以A和乙烯为起始原料,结合题中信息,选用必要的无机试剂合成苯乙酸乙酯(![]() ),参照下列模板写出相应的合成路线。_____________
),参照下列模板写出相应的合成路线。_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式正确的是( )
选项 | 实验操作 | 离子方程式 |
A | FeCl3溶液和KI溶液反应 | 2Fe3++2I-=2Fe2+ +I2 |
B | A1C13溶液中加入足量的氨水 | A13++30H- = Al(OH)3 |
C | 氯气溶于水 | Cl2 + H20=2H+ +CI-+CIO- |
D | 向稀HN03中滴加Na2S03溶液 | SO2- + 2H+=SO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】细胞中常见的化学元素有20多种,下列各组元素中,全是微量元素的是
A.Fe、Mn、Mo、S 、BB.Mo、Zn、Cu、B.、Fe
C.P、N、K、Ca、MgD.C、H、O、Ca、Mg
查看答案和解析>>
科目: 来源: 题型:
【题目】美国《科学》杂志曾报道:在40 GPa的高压下,用激光加热到1800 K,人们成功制得了原子晶体CO2,下列对该物质的推断一定不正确的是( )
A. 该原子晶体中含有极性键 B. 该原子晶体易气化,可用作制冷材料
C. 该原子晶体有很高的熔点 D. 该原子晶体硬度大,可用作耐磨材料
查看答案和解析>>
科目: 来源: 题型:
【题目】NOx会造成大气污染,在工业上采用多种方法进行处理。
I.氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知:常温下,CaSO4的沉淀溶解平衡常数数值为9.1×10-6,CaSO3的沉淀溶解平衡常数数值为3.1×10-7。
(1)NO与O3反应过程的能量变化如下:

NO被O3氧化的总反应是化合反应,该反应的热化学方程式为 ________。
(2)将CaSO3悬浊液静置,取上层清液,测得pH约为8,用化学用语解释其原因为________。
(3)用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为________。
(4)在实际吸收NO2的过程中,通过向CaSO3悬浊液中加入Na2SO4固体,提高NO2的吸收速率,从溶解平衡的角度解释其原因:________。
II. 选择性非催化还原法:该反应不使用催化剂,但必须在高温有氧下利用NH3做还原剂与 NOx 进行选择性反应:4NH3 + 4NO + O2 ![]() 3N2 + 6H2O,不同温度(T)下,反应时间(t)与NO浓度的关系如右图所示。
3N2 + 6H2O,不同温度(T)下,反应时间(t)与NO浓度的关系如右图所示。
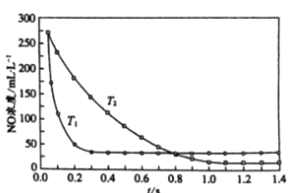
(5)判断该反应为________(填“吸热”或“放热”)反应,说明理由:________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇是重要的有机化工原料,可由乙烯水合法生产,反应的化学方程式如下:C2H4(g) + H2O(g) ![]() C2H5OH(g) ,下图为乙烯的平衡转化率与温度(T)、压强(P)的关系[起始n(C2H4) : n(H2O) =1:1]。
C2H5OH(g) ,下图为乙烯的平衡转化率与温度(T)、压强(P)的关系[起始n(C2H4) : n(H2O) =1:1]。

下列有关叙述正确的是
A. Y对应的乙醇的物质的量分数为![]()
B. X、Y、Z对应的反应速率:υ(X) >υ(Y) >υ(Z)
C. X、Y、Z对应的平衡常数数值:KX < KY <KZ
D. 增大压强、升高温度均可提高乙烯的平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com