
科目: 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是

A. 曲线①代表滴定CH3COOH溶液的曲线
B. A、C两点对应溶液均呈中性
C. B点溶液中:c(Na+) > c(OH-) > c(CH3COO-)
D. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.050mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述正确的是( )
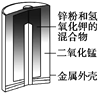
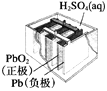
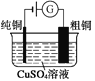
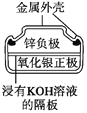
图1 碱性锌锰电池 图2 铅—硫酸蓄电池 图3 电解精炼铜 图4 银锌纽扣电池
A. 图1所示电池中,MnO2的作用是催化剂
B. 图2所示电池放电过程中,硫酸浓度不断增大
C. 图3所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图4所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目: 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法不正确的是
A. 15.6gNa2O2与过量CO2反应时,转移的电子数为0.2NA
B. 常温下,5.6g铁粉加入足量浓硝酸中反应,转移的电子数为0.3 NA
C. 常温下,4gCH4含有NA个C-H共价键
D. 分子总数为NA的ClO2和CO2混合气体中含有的氧原子数为2 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是碳酸钙(CaCO3)在25 ℃和100 ℃两种情况下,在水中的溶解平衡曲线。下列有关说法正确的是

A. CaCO3(s)![]() Ca2+(aq)+ CO32-(aq) ΔH<0
Ca2+(aq)+ CO32-(aq) ΔH<0
B. a、b、c、d四点对应的溶度积Ksp相等
C. 温度不变,蒸发水,可使溶液由a点变到c点
D. 25 ℃时,CaCO3的Ksp=2.8×10-9
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。
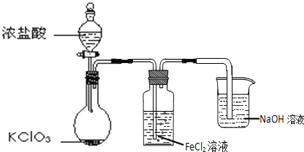
(1)NaOH溶液的作用是______。
(2)实验中,需控制氯气产生的速度,以便使FeCl2溶液转化完全。控制生成氯气速度的操作是______。
(3)开始反应后,在洗气瓶和烧杯所盛放的物质中,被氧化的是______(填化学式)。
(4)烧瓶中发生反应的化学方程式是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】海水中含有丰富的Na+、Mg2+、Cl﹣、Br﹣等化学资源。以浓缩海水为原料,通过一系列工艺流程可以提取Mg、Br2等产品。
(1)从海水中提取镁的主要步骤如下:
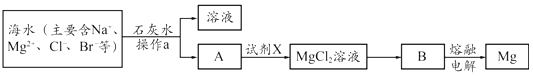
①操作a的名称是______。
②A与试剂X反应的离子方程式是______。
(2)空气吹出法是用于工业规模海水提溴的常用方法,其中一种工艺是以预先经过酸化的浓缩海水为原料,通过以下步骤提取溴。步骤Ⅰ:用氯气置换溴离子使之成为单质溴;步骤Ⅱ:通入空气和水蒸气,将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生作用转化 成氢溴酸;步骤Ⅲ:用氯气将氢溴酸氧化得到产品溴。
①下列说法正确的是______(填序号)。
a.步骤Ⅰ和步骤Ⅱ的目的是使溴富集
b.上述步骤中的反应可说明氧化性:Cl2>Br2
c.步骤Ⅰ和步骤Ⅲ发生的主要反应的原理不同
②若在步骤Ⅱ中消耗的SO2的质量为6.4×103 g,则上述过程中理论上消耗的氯气的体积在标准状况下至少是______ L。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列4种重要的有机物:
①![]() ②
②![]() ③
③![]() ④
④![]()
请回答:
(1)能发生银镜反应的是______(填序号)。
(2)能与浓硝酸在一定条件下生成烈性炸药TNT的是______(填序号)。
(3)能与③在一定条件下反应并相互缩合成高分子化合物的是______(填序号)。
(4)写出④在一定条件下发生消去反应的化学方程式:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存且溶液呈透明的是( )
A.Mg2+ 、H+ 、Cu2+ 、SO42-B.Ba2+ 、NO3- 、OH- 、CO32--
C.Ag+ 、H+ 、Cl- 、NO3-D.K+ 、H+ 、Cl- 、CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列6种与人们生产生活相关的有机物:
① ![]() (日化用品香料) ②
(日化用品香料) ② ![]() (基础化工原料)
(基础化工原料)
③ ![]() (基础化工原料) ④
(基础化工原料) ④ 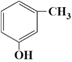 (生产农药的原料)
(生产农药的原料)
⑤ ![]() (食用香料) ⑥
(食用香料) ⑥ ![]() (食品防腐剂)
(食品防腐剂)
请回答:
(1)属于酯类的是______(填序号)。
(2)与②互为同系物的是______(填序号)。
(3)与①互为同分异构体的是______(填序号)。
(4)用系统命名法给②命名,其名称为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍。
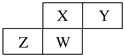
请回答下列问题:
(1)Z位于周期表中的位置______________。
(2)X、Y元素的氢化物中,较稳定性的是________(填化学式)。
(3)X的气态氢化物与其最高价氧化物对应的水化物反应生成的化合物中存在的化学键类型为_________。
(4)请写出X的最高价氧化物对应水化物的稀溶液与少量铁粉反应的离子反应方程式:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com