
科目: 来源: 题型:
【题目】下图是某有机物分子的简易球棍模型,该有机物中含C、H、O、N四种元素。下列关于该有机物的说法中错误的是( )
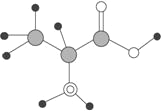
A. 分子式为C3 H7O2N B. 能发生取代反应
C. 能通过聚合反应生成高分子化合物 D. 不能跟NaOH溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生素”。为了回收利用含钢催化剂(V2O5、VOSO4及不溶性杂质),科研人员最新研制了一种离子交换法回收钒的新工艺。该工艺的主要流程如图所示:

已知:部分含钒物质在水中的溶解性:
物质 | V2O5 | VOSO4 | NH4VO3 | (VO2)2SO4 |
溶解性 | 难溶 | 可溶 | 难溶 | 易溶 |
(1)由V2O5冶炼金属钒采用铝热剂法,反应的化学方程式为:___________
(2)V2O5通常用作为反应2SO2+O2![]() 2SO3的理想催化剂,其催化的机理可能是加热时可逆地失去氧的原因,其过程可用两个化学方程式表示:_________、4V+5O2
2SO3的理想催化剂,其催化的机理可能是加热时可逆地失去氧的原因,其过程可用两个化学方程式表示:_________、4V+5O2![]() 2V2O5.
2V2O5.
(3)反应①的目的是_________.
(4)将滤液1与滤液2混合后用氯酸钾氧化,氯元素被还原为最低价,其反应的离子方程式为______.
(5)反应③的沉淀率(又称沉钒率) 是回收钒的关键之一,下图是反应温度与沉钒率的关系图,则控制温度的方法是____________.

(6)反应④在NH4VO3的焙烧过程中,固体质量的减少值(纵坐标) 随温度变化的曲线如图2所示,则其分解过程中_______(填字母代号)。

A.先分解失去H2O,再分解失去NH3
B.先分解失去NH3, 再分解失去H2O
C.同时分解失去H2O 和NH3
D.同时分解失去H2和N2和H2O
(7)全钒电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+![]() VO2++H2O+V3+。电池充电时阳极的电极反应式为__________
VO2++H2O+V3+。电池充电时阳极的电极反应式为__________
查看答案和解析>>
科目: 来源: 题型:
【题目】现有a mol/L 的NaX和b mol/L的NaY两种盐溶液。下列说法正确的是
A. 若a=b且c(X-)= c(Y-)+ c(HY),则HX为强酸
B. 若a=b且pH(NaX)>pH(NaY),则c(X-)+ c(OH-)> c(Y-)+ c(OH-)
C. 若a>b且c(X-)= c(Y-),则酸性HX>HY
D. 若两溶液等体积混合,则c(Na+)="(a+b)" mol/L(忽略混合过程中的体积变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位。请回答下列问题:

(1)图中X是________,Ⅰ在小麦种子中主要是指__________。
(2)在病毒中,携带遗传信息的物质是________________。(填序号)
(3)图中B是______,P的结构通式为________________________。
(4)导致地球上生物多种多样的直接原因是[ ] _________(填序号和名称)结构的多样性。
(5) 若P的平均相对分子质量为100,通过脱水合形成2条肽链,其中肽键的数目为10个,则这2条肽链的相对分子质量为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.5%的ZnS和12.8%的CuS,某同学以该废催化剂为原料,回收其中的锌和铜。采用的实验方案如下:

已知:1.步骤①中发生的化学反应为非氧化还原反应 2.滤渣2的主要成分是SiO2和S,下列说法不正确的是
A. 步骤①,最好在通风橱中进行
B. 步骤①和③,说明CuS不溶于稀硫酸而ZnS溶于稀硫酸
C. 步骤③,涉及的离子反应为CuS+H2O2+2H+![]() Cu2++S+2H2O
Cu2++S+2H2O
D. 步骤②和④,均采用蒸发结晶的方式获取溶质
查看答案和解析>>
科目: 来源: 题型:
【题目】在某2 L恒容密闭容器中充入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+Y(g)![]() 3Z(g),反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
3Z(g),反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )

A. M点时,Y的转化率最大
B. 升高温度,平衡常数减小
C. 平衡后充入Z,达到新平衡时Z的体积分数增大
D. W、M两点Y的正反应速率相同
查看答案和解析>>
科目: 来源: 题型:
【题目】反应2FeCl3+Cu===2FeCl2+CuCl2可用于制作印刷电路板。下列关于该反应的说法正确的是( )
A.Cu为还原剂B.FeCl3被氧化
C.Cu得到电子D.FeCl3发生氧化反应
查看答案和解析>>
科目: 来源: 题型:
【题目】Be(OH)2是两性的,跟强酸反应时生成Be2+,跟强碱反应时生成BeO22—。现有三份等物质的量浓度、等体积的BeCl2、MgCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mol)的关系如图所示,则与BeCl2、MgCl2、AlCl3三种溶液对应的图像正确的是( )

A. ⑤③① B. ②③④ C. ③⑤④ D. ③②①
查看答案和解析>>
科目: 来源: 题型:
【题目】加成反应是有机化学的一类重要的反应,下列反应属于加成反应的是 ( )
A. 乙醇与金属钠作用
B. 乙烯通入溴水中
C. 乙烯通入酸性高锰酸钾溶液中
D. 油脂在碱性条件下加热,制取肥皂
查看答案和解析>>
科目: 来源: 题型:
【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
c(mol·L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4) | 0.20 | a | 0.10 | C | d | e |
c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为________________________________。
(2)20s时,N2O4的的浓度为__________mol·L-1,0~20s内N2O4的平均反应速率为_____________。
(3)该反应的平衡常数表达式K=____________,80℃反应K值为___________保留2位小数)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时______________。
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
(5)要增大该反应的K值,可采取的措施_________
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂 D.升高温度
(6)下图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线_______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com