
科目: 来源: 题型:
【题目】下列物质属于电解质的一组是( )
A.CO2、NH3、HCl
B.H2SO4、HNO3、BaCl2
C.H3PO4、H2O、Cu
D.液态KNO3、NaOH溶液、CH3COOH
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时,4v正(O2)=5v逆(NO)
B. 若单位时间内生成xmol NO的同时,消耗xmol NH3,则反应达到平衡状态
C. 若有5 mol O===O键断裂,同时有12 mol H—O键形成,此时必为化学平衡状态
D. 化学平衡时,化学反应速率关系是2v正(NH3)=3v逆(H2O)
查看答案和解析>>
科目: 来源: 题型:
【题目】以A(C2H2)为原料合成食用香料E和吡咯(pyrrole)的路线如图所示,部分反应条件及产物略去。其中D在一定条件下可被氧化成酮。
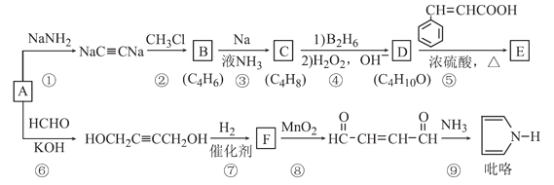
回答下列问题:
(1)A的名称是_________;已知C是反式产物,则C的结构简式为_________。
(2)⑥的反应类型是_________,⑧的反应类型是__________。
(3)F含有的官能团的名称是________。
(4)反应⑤的化学方程式为__________。
(5)肉桂酸(![]() )的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有_____种(不考虑顺反异构)。与D互为同分异构体,且核磁共振氢谱有面积比为2:3的两组峰的有机物的结构简式是___________。
)的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有_____种(不考虑顺反异构)。与D互为同分异构体,且核磁共振氢谱有面积比为2:3的两组峰的有机物的结构简式是___________。
(6)参照上述合成路线,设计一条由A和乙醛为起始原料制备2,5-二甲基吡咯(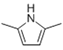 )的合成路线____。
)的合成路线____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下面有关变化过程,不属于氧化还原反应的是( )
A.烧菜用过的铁锅,经放置常出现红棕色斑迹
B.用煤气灶燃烧天然气为炒菜提供热量
C.牛奶久置空气中变质腐败
D.向沸水中滴入FeCl3饱和溶液,适当加热,制备胶体
查看答案和解析>>
科目: 来源: 题型:
【题目】已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)常温下,在pH =5的稀醋酸溶液中,c(CH3COO-)=_______________________(不必化简)。下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是_________________
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)________________V(醋酸),反应的最初速率为:υ(盐酸)___________υ(醋酸)。(填写“>”、“<”或“=”)
(3)常温下,向体积为Va mL,pH为3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系为:_________________。
(4)常温下,将0.1 mol/L盐酸和0.1 mol/L醋酸钠溶液混合,所得溶液为中性,则混合溶液中各离子的浓度按由大到小排序为__________________________________。
(5)已知:90℃时,水的离子积常数为Kw=3.8×10-13,在此温度下,将pH=3的盐酸和pH=11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=______________(保留三位有效数字)mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
(1)不同温度下的平衡转化率与压强的关系如图所示。

①该反应△H 0,△S 0(填“>”或“<”),则该反 自发进行(填“一定能”、“一定不能”、“不一定”)实际生产条件控制在250℃、l.3×l04kPa左右,选择此压强的理由是 。
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.l mol·L -1。
①该反应的平衡常数K= :
②在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有关说法正确的是 (填序号)。
A.氢气的浓度减少
B.正反应速率加快,逆反应速率也加快
C.甲醇的物质的量增加
D.重新平衡时n(H2)/n(CH3OH)增大
③若保持同一反应温度将起始物质改为a mol CO、b mol H2、c mol CH30H,欲使平衡混合物中各组成与原平衡相同,则a、b应满足的关系为 ,且欲使开始时该反应向逆反应方向进行,c的取值范围是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化锂是一种优良的贮氢材料,它是一种紫色或红色的晶状固体,在空气中长期暴露,最终会变成碳酸理。氮化理易水解生成氢氧化锂和氨气,在空气中加热能剧烈燃烧,特别是细粉末状的氮化锂: 锂与氨反应生成LiNH2和H2实验室用以下装置制取干燥、纯净的N2并与金属锂(密度为0.534g/cm3) 反应制取氮化锂。

回答下列问题:
(1)连接好装置进行实验前必须______________
(2)实验步骤如下:
①装药品 ②点燃C处酒精灯 ③点燃E处酒精灯 ④打开A中分液漏斗
正确的先后顺序为________(填序号)
(3)装置A是制备氨气的简易装置烧瓶中固体是:_______;D装置的作用是_______.
(4)写出C中化学方程式为___________
(5)将12.0g锂放入E反应,实验结束后称得E装置增加了7.0g,计算生成氮化锂的质量分数为________(结果保留一位小数)。
(6)设计简单实验证明E中产物为氮化锂:_________
查看答案和解析>>
科目: 来源: 题型:
【题目】氰[(CN)2]的化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间,下列有关反应方程式不正确的是
A. (CN)2和NaOH溶液反应:(CN)2+2OH-=CN-+CNO-+H2O
B. MnO2和HCN反应:MnO2+4HCN(浓)![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2CN-=2Cl-+(CN)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com