
科目: 来源: 题型:
【题目】有机玻璃是一种重要的塑料,有机玻璃的单体A(C5H8O2)不溶于水,并可以发生以下变化:

请回答:
(1)B分子中含有的官能团是________、________。
(2)由B转化为C的反应属于________(选填序号)。
①氧化反应 ②还原反应 ③加成反应 ④取代反应
(3)C的一氯代物D有两种,C的结构简式是________。
(4)由A生成B的化学方程式是___________________________________。
(5)有机玻璃的结构简式是______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】空气吹出法工艺是目前“海水提溴”的最主要方法之一,其工艺流程如图所示。

(1)“苦卤”到“含Br2的海水”过程____(填“是”或“不是”)氧化还原反应。
(2)步骤④利用了S02的还原性,反应的离子方程式为____。
(3)步骤⑥的蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,其原因是____。
(4)若处理1 m3海水需要消耗0.45 molSO2,不考虑转化过程中溴的损耗,则海水中溴离子的物质的量浓度为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z是四种原子序数依次增大的短周期元素,W、X两种元素可组成W2X和W2X2两种常见的无色液体化合物,Y2X2为淡黄色固体化合物,Z的原子序数是X的原子序数的两倍。请回答下列问题:
(1)Z元素的名称是____。
(2)W、X、Y三种元素形成的化合物是________(用化学式表示)。
(3)写出Y2XZ的电子式____。
(4)写出W2X2和ZX2反应的化学方程式____。
(5)W2和X2是组成某种燃料电池的两种常见物质,如图所示,通入X2的电极是____(填“正极”或“负极”),写出通入W2的电极的电极反应式____。

查看答案和解析>>
科目: 来源: 题型:
【题目】某粗铜产品中含有Zn、Ag、Au等杂质,如图所示,用CH3OH-碱性燃料电池电解硫酸铜溶液。闭合电键K进行电解。下列说法中不正确的是( )

A. 左池负极反应式为CH3OH -6e-+8OH-=CO32-+ 6H2O
B. 通电一段时间后,Ag、Au杂质金属沉积在电解槽底部
C. 若粗铜电极质量减少6.4g,则纯铜电极增重大于6.4g
D. 电解过程中右池纯铜和粗铜分别为阴极和阳极
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A的结构简式为![]() ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。

请回答下列问题:
(1)指出反应的类型:A→C:_________________;
(2)在A~E五种物质中,互为同分异构体的是________________(填代号);
(3)写出由A生成B的化学方程式:_____________________________;
(4)写出D与NaOH溶液共热反应的化学方程式_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是______(填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
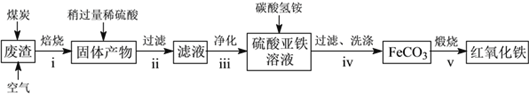
回答下列问题:
①在步骤i中产生的有毒气体可能有__________________。
②在步骤iii操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上将Al3+沉淀完全,则溶液的pH为____________。
③步骤iv中,生成FeCO3的离子方程式是_________________。
(3)氯化铁溶液称为化学试剂中的“多面手”,向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式_________________。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释:___________________。
(4)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是________________。
②如今基于普鲁士蓝合成原理可检测食品中CN-,方案如下:
![]()
若试纸变蓝则证明食品中含有CN-,请解释检测时试纸中FeSO4的作用:
_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】聚氯乙烯简称PVC,是当今世界上产量最大、应用最广的热塑性塑料之一。
(1)工业上以乙烯和氯气为原料合成PVC的流程如下:
乙烯![]() 1,2-二氯乙烷(CH2ClCH2Cl)
1,2-二氯乙烷(CH2ClCH2Cl)![]() 氯乙烯(CH2=CHCl)
氯乙烯(CH2=CHCl)![]() PVC
PVC
①氯乙烯的分子式为____。
②乙烯生成1,2-二氯乙烷的反应类型是____。
③氯乙烯生成PVC的化学方程式为____。
(2)下列有关PVC的说法正确的是___(填字母)。
A.PVC的单体是CH3CH2Cl
B.PVC是高分子化合物
C.PVC能够使溴的四氯化碳溶液褪色
D.PVC易降解
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,10 mL 0.40 mol/LH2O2溶液发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 | a |
下列叙述正确的是(溶液体积变化忽略不计)
A. 0~6 min的平均反应速率:v(H2O2)≈3.3×10-2 mol·L-l·min-l
B. 反应到6 min时,c(H2O2)=0.30mol·L-l
C. 反应到6 min时,H2O2分解了60%
D. 12 min时,a=33.3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是
A. NH3易液化,可用作制冷剂
B. 浓H2SO4具有脱水性,可用来干燥HCl
C. FeCl3溶液呈酸性,可用于腐蚀电路板上的Cu
D. 碳酸钡不溶于水,可作钡餐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com