
科目: 来源: 题型:
【题目】质子交换膜燃料电池(简称:PEMFC),又称固体高分子电解质燃料电池,是一种以含氢燃料与空气作用产生电力与热力的燃料电池,膜极组和集电板串联组合成一个燃料电池堆。目前,尤以氢燃料电池倍受电源研究开发人员的注目。它的结构紧凑,工作温度低(只有80℃),启动迅速,功率密度高,工作寿命长。工作原理如图,下列说法正确的是

A. 可用一氧化碳代替图中氢气形成质子交换膜燃料电池
B. B极的电极反应式为O2+4H++4e-=2H2O
C. 用该电池作为精炼铜的电源时,A极与粗铜电极相连
D. 当外电路中转移0.1mole-时,通过质子交换膜的H+数目为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】铝镁合金已成为飞机制造、化工生产等行业的重要材料.某研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其他元素)中镁的质量分数,设计下列实验方案进行探究。填写下列空白。
[实验方案]
将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况下(约20℃,1.01×105 Pa)的体积。
[问题讨论]
(1)同学们拟选用下列实验装置完成实验:

①你认为最简易的装置其连接顺序是:
A接(____)( )接( )( )接( )( )。(填接口字母,可不填满)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因_______________________________。
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了如图所示的实验装置。

(碱式滴定管上的刻度数值上小下大)
①装置中导管a的作用是____________________________________________________。
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL.则产生氢气的体积为________ mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。

(1)A中试剂为________。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是____________________。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B中滴加足量试剂。上述操作的顺序是________(填序号);记录C的液面位置时,除平视外,还应________。
(4)B中发生反应的化学方程式为__________________________。
(5)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为c g,则铝的相对原子质量为________。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________(填“偏大”“偏小”或“不受影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A为常见的金属单质,根据下图所示的关系,回答下列问题。

(1)确定A、B、C、D、E、F的化学式,A为________,B为________,C为________,D为________,E为________,F为________。
(2)写出反应⑧的化学方程式和反应④、⑤的离子方程式。
⑧_____________________________________________________;
④_____________________________________________________;
⑤_____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A. 0.1 mol·L-1的Na2CO3溶液中:c(OH-)=c(HCO![]() )+c(H+)+c(H2CO3)
)+c(H+)+c(H2CO3)
B. 25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH
C. 常温下将10mlpH=4的醋酸溶液稀释至100ml,所得溶液4<pH<5
D. 向NaAlO2溶液中滴加NaHCO3溶液相互促进水解,有沉淀和气体生成
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,向一固定容积的密闭容器中加入1molM和2molN,发生反应:M(g)+2N(g)![]() 3Q(g)+2R(s),△H<0,达到平衡时生成了1.8 molQ
3Q(g)+2R(s),△H<0,达到平衡时生成了1.8 molQ
(1)若维持容器的体积和温度不变,反应从逆反应方向开始,Q和R按一定的物质的量作为起始反应物质,达到平衡时Q仍为1.8mol。则R的起始物质的量n(R)应满足的条件是:n(R)_________mol。
(2)若升高平衡体系温度,当再次达到平衡后,测得两次平衡条件下混合气体的平均相对分子质量未发生改变,试解释形成这种结果的可能原因是:_______________。
(3)若将容器改为容积可变的容器,在一定温度和常压下,建立上述平衡之后,M的物质的量浓度为a mol·L-1,现持续增大压强。
①当压强为原来的1.5倍时,平衡时M的物质的量浓度为m mol·L-1,测得m=1.5a;
②当压强为原来的10倍时,平衡时M的物质的量浓度为n mol·L-1,测得n>10a;
试解释形成这种结果的可能的原因:
①1.5倍时:_____________________________________________;
②10倍时:_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氰基烯酸酯在碱性条件下能快速聚合为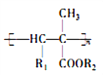 ,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
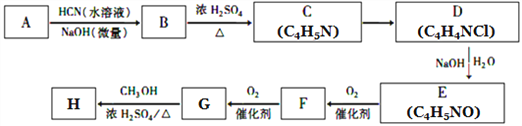
已知:①A的相对分子量为58,氧元素质量分数为0. 276,核磁共振氢谱显示为单峰;
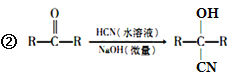
回答下列问题:
(1)A的化学名称为____________。
(2)C的结构简式为________________,F中的含氧官能团名称是________________。
(3)由E生成F的反应类型为_____________,由G生成H的反应类型为_____________。
(4)由G生成H的化学方程式为________________________________。
(5)写出A的能够发生银镜反应的同分异构体的结构简式______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1molCl2溶于水后溶液中Cl2、HClO、ClO-、Cl-四种粒子总数为2NA
B. 6.4gCu与足量浓硝酸反应生成NO2分子数目为NA
C. 1mol淀粉(C6H10O5)n水解后产生的葡萄糖分子数目为NA
D. 标准状况下,2molNa2O2与44.8LSO2完全反应,转移的电子数目为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com