
科目: 来源: 题型:
【题目】二氧化锆(ZrO2)是最重要的氧离子固体电解质,用于制造燃料电池、氧气含量测定仪等。可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2;含有少量Fe2O3、Al2O3、SiO2杂质)通过如工艺流程法制得。
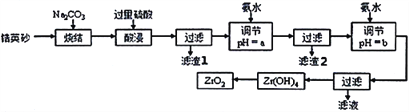
已知:①ZrO2具有两性,高温与纯碱共熔生成可溶于水的Na2ZrO3,与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
金属离子 | Fe3+ | Al3+ | ZrO2+ |
开始沉淀时pH | 1.9 | 3.3 | 6.2 |
沉淀完全时pH | 3.2 | 5.2 | 8.0 |
请回答下列问题:
(1)已知Zr元素的原子序数是40,请写出它在周期表中的位置:____________________________。
(2)烧结时ZrSiO4发生反应的化学方程式为__________________________;滤渣1的化学式为__________。
(3)调节pH=a时,a的范围应该是__________________;用氨水调节pH=b时,所发生反应的离子方程式为_______________________________________。
(4)本题的流程中,一共有三步过滤操作,北中最后一步过滤所得的Zr(OH)4沉淀需要洗涤,证明该沉淀已经洗涤干净的最佳操作方法是:______________________________________。
(5)工业上用铝热法冶炼锆,写出以ZrO2通过铝热法制取锆的化学方程式:________________。
(6)一种新型燃料电池用掺杂Y2O3的ZrO2晶体作电解质在熔融状态下传导O2-,一极通入空气,另一极通入乙烷,写出负极的电极反应式:________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】中国女药学家屠呦呦因创制新型抗疟药——青蒿素(结构如图)和双氢青蒿素的贡献,挽救了全球特别是发展中国家的数百万人的生命”。青蒿素是从植物黄花蒿茎叶中提取的,荣获2015年诺贝尔奖生物学或医学奖。下列有关青蒿素的叙述不正确的是

A. 分子式为C15H22O5
B. 它在乙醚中的溶解度大于在水中的溶解度
C. 能发生取代反应、水解反应、加成反应,不能发生氧化反应
D. 该物质不稳定,容易受到热和还原性物质的影响而发生变质
查看答案和解析>>
科目: 来源: 题型:
【题目】右图1为甲烷和O2构成的燃料电池示意图,电解质溶液为KOH溶液,图2为电解AlCl3溶液的装置,电极材料均为石墨。用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。下列说法正确的是
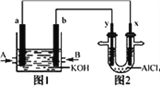
A. 图2中Y电极为阴极
B. 图2中总反应的化学方程式为:2AlCl3+6H2O2![]() 2Al(OH)3↓+3Cl2↑+3H2↑
2Al(OH)3↓+3Cl2↑+3H2↑
C. 图1中电解质溶液的pH增大
D. 图1中的a 电极反应式为:CH4-8e-+8OH-=CO2+6H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】B、C、N、O、Si、S 是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在

(1)Si位于元素周期表第______周期______族;基态硼原子的电子排布式为______;C、N、Si元素原子的第一电离能由大到小的顺序为______。
(2)BF3与一定量的水可形成如图1晶体R,晶体R中各种微粒间的作用力包含______(填字母)。
a.离子键 b.共价键 c.范德华力 d.金属键
(3)乙二胺(H2N﹣CH2﹣CH2﹣NH2)与CuCl2溶液可形成配离子(结构如图2)。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是______。
(4)在25℃、101kpa,NO2(g)与SO2(g)反应生成 SO3(g)和 NO(g),已知每生成1gSO3(g)放出热量 0.52kJ,该反应的热化学方程式是______。
(5)硼砂(Na2B4O710H2O)可用作清洁剂或杀虫剂,易溶于水.在酸性溶液中会生成H3BO3,该反应的离子方程式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,用0.200mol·L-1NaOH溶液分别滴定20.0mL0.200 mol·L-1的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是

A. Ⅱ表示的是滴定醋酸的曲线
B. pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C. V(NaOH)=20.00mL时,两份溶液中c(Cl-)=c(CH3COO-)
D. V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO-)> c(OH-)> c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】己知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如下图所示,下列说法一定正确的是
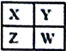
A. 若X元素在自然界中存在同素异形体,则W在同周期元素中,原子半径最小
B. 若HmXOn为强酸,则X 的氢化物溶于水一定显酸性(m、n均为正整数)
C. 若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
D. 若四种元素均为非金属,则Y元素在化合物中不可能显示正化合价
查看答案和解析>>
科目: 来源: 题型:
【题目】为了从KCl和MnO2的混合物中回收MnO2,下列操作顺序正确的是(已知MnO2为黑色难溶于水的固体)( )
A.溶解 过滤 蒸发 洗涤B.溶解 过滤 洗涤 干燥
C.溶解 过滤 蒸发 干燥D.溶解 洗涤 过滤 干燥
查看答案和解析>>
科目: 来源: 题型:
【题目】TiCl4是制备钛及其化合物的重要中间体,某小组同学利用下列装置在实验室制备TiCl4,设计实验如下(夹持装置略去):

相关信息如下表所示。
化合物 | 熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | 水溶性 |
TiCl4 | -25 | 136 | 1.5 | 易水解生成难落于水的物质,能熔于有机溶剂 |
CCl4 | -23 | 76.8 | 1.6 | 难溶于水 |
请回答下列问题:
(1)按 照气流由左到右的方向,上述装置合理的连接顺序为a →____ →____ →f→g→_____ →____→d→e→j。(填仪器接口字母)_____________
(2)装置A中导管m的作用是________________________________。
(3)装置D中除生成TiCl4 外,同时生成一种气态不成盐氧化物,该反应的化学方程式为________________________________。
(4)设计实验证明装置E中收集到的液体中含有TiCl4:________________________________。
(5)制得的TiCl4中常含有少量CCl4,从混合液体中分离出TiCl4的操作名称为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列生活生产中常见的物质里含有的有机物属于高分子化合物的是
A. 植物中所含的非常复杂的叶绿素 B. 石油分馏所得的重油中含有的C16H34
C. 植物油水解得到的高级脂肪酸 D. 芹菜中含有的粗糙的纤维素
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 碳酸钠溶液和碳酸氢钠溶液都能与澄清石灰水反应产生沉淀
B. 二氧化硫能使酸性高锰酸钾溶液紫红色褪去
C. 实验室能用二氧化锰和稀盐酸共热制氯气
D. 常温下铝片不能溶于浓硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com