
科目: 来源: 题型:
【题目】关于蛋白质的叙述,错误的是( )
A. 人体血浆中含有浆细胞分泌的蛋白质 B. DNA和蛋白质是染色体的组成成分
C. rRNA能参与蛋白质的生物合成 D. 核糖体上合成的蛋白质不能在细胞核发挥作用
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于漂白粉的叙述正确的是( )
A.漂白粉的有效成分是Ca(ClO)2和CaCl2
B.漂白粉在空气中久置后会变质失效
C.漂白粉的有效成分Ca(ClO)2不稳定,易分解
D.在使用漂白粉时要加盐酸
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室检验SO2中混有CO2的装置如图所示。下列说法正确的是
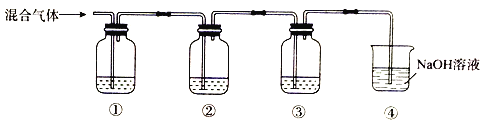
A. ①、②、③中可依次盛放饱和NaHCO3溶液、品红溶液、澄清石灰水
B. ②的主要作用是除去SO2
C. ③中观察到的现象是先有白色沉淀,当沉淀最多后再不断溶解
D. 该装置也可用于检验NO2中混有NO
查看答案和解析>>
科目: 来源: 题型:
【题目】如图甲是利用一种微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是( )

A. 铜电极应与X相连接
B. H+透过质子交换膜由右向左移动
C. M电极反应式为CO(NH2)2+H2O-6e-===CO2↑+N2↑+6H+
D. 当N电极消耗0.25 mol气体时,则理论上铁电极增重16 g
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)写出下列反应的化学方程式,用双线桥法标明电子转移的方向和数目,并注明“被氧化”、“被还原”。
①Fe2O3与CO在高温下的反应:___________________________________。
②KClO3与MnO2在共热条件下反应:________________________________。
③H2S气体和SO2气体反应生成S和水:______________________________。
(2)写出下列反应的离子方程式,并用单线桥法标明电子转移的方向和数目。
①Cu和AgNO3溶液反应:________________________________________。
②实验室制Cl2的反应为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O:___________________________。
MnCl2+Cl2↑+2H2O:___________________________。
③向FeCl2溶液中通入Cl2生成FeCl3:____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu + 8HNO3 (稀)=3Cu(NO3)2 + 2NO↑+ 4H2O。
(1)被氧化的元素是_______,被还原的元素是__________,发生氧化反应的物质是________,发生还原反应的物质是______________。
(2)用双线桥法表示反应电子得失的方向和数目:__________________________________。
(3)用单线桥法表示反应电子得失的方向和数目:__________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关纯羊毛线的叙述,正确的是( )
A. 组成纯羊毛线的基本单位是核苷酸
B. 纯羊毛线形成过程中一定有水产生
C. 纯羊毛服装可以用加入蛋白酶的洗衣粉清洗
D. 纯羊毛线中一定含有的化学元素是C、H、O、N、P
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20 mL 0.1 mol·L-1的盐酸中逐滴加入0.1 mol·L-1的氨水,溶液pH的变化与加入氨水的体积关系如图所示。下列叙述正确的是
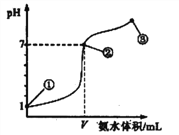
A. V=20mL
B. 在点①所示溶液中:c(Cl-)=c(H+)
C. 在点②所示溶液中:c(H+)=c(NH3·H2O)+c(OH-)
D. 在点②、③之间可能存在:c(NH4+)>c(Cl-)=c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:25℃时,Ksp[Zn(OH)2]=1.0×10-18,Ka(HCOOH)=1.0×10-4。该温度下,下列说法错误的是
A. Zn(OH)2溶于水形成的饱和溶液中c(Zn2+)>1.0×10-6 mol·L-l
B. HCOO-的水解常数为1.0×10-10
C. 向Zn(OH)2悬浊液中加入HCOOH,溶液中c(Zn2+)增大
D. Zn(OH)2+2HCOOH![]() =Zn2++2HCOO-+2H2O的平衡常数K=100
=Zn2++2HCOO-+2H2O的平衡常数K=100
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用软锰矿浆烟气脱硫吸收液制取电解锰,并利用阳极液制备高纯碳酸锰、回收硫酸铵的工艺流程如下(软锰矿的主要成分是MnO2,还含有硅、铁、铝的氧化物等杂质):
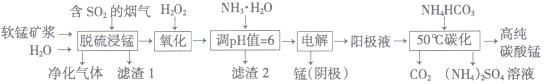
已知:Fe(OH)3的Ksp=l.0×10-38,Al(OH)3的Ksp=1.0×10-34
(1)一定温度下, “脱硫浸锰”主要产物为MnSO4,生成该产物的化学方程式为_________。
(2)常温下,调节pH=6时,得到的“滤渣2”主要成分为Fe(OH)3和_____(化学式),此时溶液中的Fe3+物质的量浓度为_________ 。
(3)“电解”时用惰性电极,阳极的电极反应式为_______________。
(4)“50℃碳化”得到高纯碳酸锰,反应的离子方程武为____________________。“50℃碳化”时加入过量NH4HCO3,可能的原因:①使MnSO4充分转化为MnCO3;②________________;③________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com