
科目: 来源: 题型:
【题目】等质量的两份锌粉a、b,分别加入两支相同的试管中,然后加入等体积等物质的量浓度且均过量的稀硫酸,同时向a中加入少量CuSO4溶液,则产生氢气的体积(V)与时间(t)的关系用图像表示如下,其中正确的是( )
A. 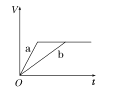 B.
B. 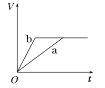 C.
C. 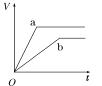 D.
D. 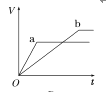
查看答案和解析>>
科目: 来源: 题型:
【题目】下列电离方程式不正确的是( )
A.H2SO4═2H++SO42-B.NH4NO3=NH4++NO3-
C.NaHCO3═Na++H++CO32-D.Ba(OH)2═Ba2++2OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】对下列物质分类全部正确的是( )
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氧 ⑥KClO3
A.碱--①④B.纯净物--③④C.盐--①⑥D.混合物--②⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.棕色集气瓶中装有Cl2和O2,可用观察颜色的方法把它们区别开来
B.棕色集气瓶中装有Cl2和O2,可用加水的方法把它们区别开来
C.某混合气体若为无色气体,则混合气体中肯定不含大量Cl2
D.某混合气体若为无色气体,则混合气体中肯定不含大量O2
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,甲,乙两个容器中,分别加入0.1mol/L的NaCl溶液与0.1mol/L的AgNO3溶液后,以Pt为电极进行电解时,下列说法中正确的是( )
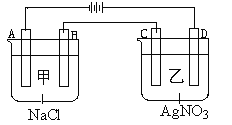
A. 电解后两烧杯中溶液的pH均增大
B. 在A、B、C、D各电极上生成物的物质的量之比为:2:2:4:1
C. 电解过程中,A电极上发生还原反应,2Cl--2e-=Cl2
D. 电解后向溶液中加入适量AgNO3固体,可使溶液恢复到原来的浓度和pH
查看答案和解析>>
科目: 来源: 题型:
【题目】我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。 右图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。下列说法不正确的是( )

A. 腐蚀过程中,负极是c
B. 正极反应是 O2+ 4e-+2H2O = 4OH-
C. 若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为0.224L(标准状况)
D. 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大。第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)A的最高价含氧酸根离子中其中心原子采取 杂化。
(3)与A、B形成的阴离子(AB-)互为等电子体的分子有 。
(4)基态D原子的核外电子排布式为 ,下图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比为 。

(5)向D的高价态硫酸盐溶液中逐滴滴加B的氢化物水溶液至过量,先出现沉淀,最后沉淀溶解形成溶液。写出此沉淀溶解的离子方程式:_ ___。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,下列叙述正确的是 ( )
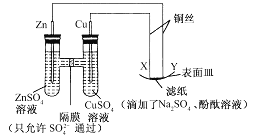
A. Y与滤纸接触处有氧气生成
B. X为正极,发生还原反应
C. SO42-从右侧透过隔膜迁移到左侧
D. X与滤纸接触处变红
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E五种短周期元素,原子序数依次增大。A与B、C分别构成电子数相等的化合物W、K,且W是一种能产生温室效应的气体;D元素最外层电子数是次外层电子数的3倍。A、D、E构成化合物Y,A、B、C、D构成化合物X,且X、Y均为阳离子和阴离子个数比是1∶1的离子化合物。回答下列问题:
(1)推断元素D为___________。
(2)Y的电子式为_______;物质W为_______,其晶体中存在的作用力有_______。
(3)与E同主族且为第7周期的元素原子序数为________。
(4)A与C形成的K是生产某种常用肥料的重要原料,写出其被催化氧化的反应方程式______。
(5)X、Y按1∶2反应的离子方程式为____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I、请用勒·夏特列原理解释如下生活中的常见现象:打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。_______________________________________________________________
II、一密封体系中发生下列反应:N2 +3H2 ![]() 2NH3 +Q,下图是某一时间段中反应速率与反应进程的曲线关系图:
2NH3 +Q,下图是某一时间段中反应速率与反应进程的曲线关系图:

回答下列问题:
(1)处于平衡状态的时间段是_______________________
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化?____________、 ____________、____________
(3)下列各时间段时,氨的百分含量最高的是(______)
A、t0~t1 B、t2~t3 C、t3~t4 D、t5~t6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com