
科目: 来源: 题型:
【题目】一定条件下存在反应:2SO2(g)+O2(g)═2SO3(g),△H<0.现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如图所示投料,并在400℃条件下开始反应.达到平衡时,下列说法正确的是( )

A. 容器Ⅰ、Ⅲ中平衡常数相同
B. 容器Ⅱ、Ⅲ中正反应速率相同
C. SO3的体积分数:Ⅱ<Ⅲ
D. 容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1
查看答案和解析>>
科目: 来源: 题型:
【题目】废水废气对自然环境有严重的破坏作用,大气和水污染治理刻不容缓。
(1)某化工厂产生的废水中含有Fe2+、Mn2+等金属离子,可用过硫酸铵[(NH4)2S2O8]氧化除去。
①过硫酸铵与Mn2+反应生成MnO2的离子方程式为________________。
②温度与Fe2+、Mn2+氧化程度之间的关系如图1所示:

图1
实验过程中应将温度控制在________________。Fe2+与Mn2+被氧化后形成胶体絮状粒子,常加入活性炭处理,加入活性炭的目的为________________。
③H2O2也有较强氧化性,在实际生产中不用H2O2氧化Mn2+的原因是________________。
(2)利用某分子筛作催化剂,NH3可脱除废气中NO、NO2,其反应机理如图2所示。A包含物质的化学式为N2和________________。


图2 图3
(3)工业上废气中SO2可用Na2CO3溶液吸收,反应过程中溶液组成变化如图3所示。
①吸收初期(图中A点以前)反应的化学方程式为________________。
②C点高于B点的原因是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种碱性“二甲醚(CH3OCH3)直接燃料电池”具有启动快、能量密度高、效率好等优点。其电池总反应为![]() ,下列说法不正确的是
,下列说法不正确的是
A. 电极正极可用多孔碳材料制成
B. 电池负极发生的反应为![]()
C. 理论上,1mol二甲醚放电量是1mol甲醇(![]() )放电量的2倍
)放电量的2倍
D. 电池工作时, ![]() 向电池负极迁移
向电池负极迁移
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关甲苯的实验事实中,能说明苯环对侧链性质产生影响的是( )
A. 甲苯燃烧产生带浓烟的火焰
B. 甲苯能使酸性KMnO4溶液褪色
C. Cl2既能取代甲苯中苯环上的氢原子,也能取代甲基上的氢原子
D. 甲苯能与H2发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】能用离子方程式H++OH﹣=H2O表示的反应是( )
A.稀醋酸和氢氧化钾反应
B.硫酸氢钠和烧碱溶液反应
C.稀盐酸和氢氧化铜反应
D.稀硫酸和氢氧化钡溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)(已知:2SO2+O2![]() 2SO3),反应过程中的能量关系可用如图简单表示(图中的△H 表示生成1mol产物的数据). 下列说法正确的是( )
2SO3),反应过程中的能量关系可用如图简单表示(图中的△H 表示生成1mol产物的数据). 下列说法正确的是( )

A. S8的燃烧热△H=﹣a kJ·mol﹣1
B. 1 mol SO2和过量 O2反应可释放出 b kJ 的热量
C. 已知1个S8分子中有8个S﹣S,S=O的键能为d kJ·mol﹣1,O=O的键能为e kJ·mol﹣1,则S8分子中S﹣S的键能为(2d﹣a﹣e) kJ·mol﹣1
D. 若使用V2O5作催化剂,当SO2(g)转化生成1mol SO3(g)时,释放的热量小于b kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g),反应过程如下图所示,下列说法正确的是
2NH3(g),反应过程如下图所示,下列说法正确的是

A. t1 min时正、逆反应速率相等
B. X曲线表示NH3的物质的量随时间变化的关系
C. 0~8 min,H2的平均反应速率v(H2)=3/4 mol·L-1·min-1
D. 10~12 min,N2的平均反应速率v(N2)=0.25 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】利用锌冶炼废渣(ZnSO4、CuSO4、FeSO4、FeS2、Al2O3、SiO2)制备ZnSO4和Fe2O3的实验流程如下:

已知:“碱浸”时,NaOH溶液浓度越大越粘稠,越容易生成铝硅酸钠沉淀。
(1) “水浸”阶段需在70~80℃条件下进行,适宜的加热方式为________________。
(2)“氧化”阶段是将Fe2+氧化后进一步生成Fe(OH)3,从反应产物的角度分析,以氯水替代H2O2的缺点是①使ZnSO4中混有ZnCl2;②________________。
(3)“灼烧”时FeS2发生反应的化学方程式为________________。使用的装置如右图,仪器a的名称为________________。
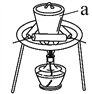
(4) “碱浸”阶段,在其它条件不变的情况下,所得固体中Fe2O3含量随NaOH溶液的浓度的增大而增大,但当氢氧化钠浓度大于12 mol·L-1时,Fe2O3含量反而降低,其原因是________________。
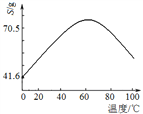
(5)“滤液Ⅰ”溶质主要是ZnSO4和CuSO4。已知硫酸锌晶体的溶解度随温度变化如右图,请设计从“滤液Ⅰ”中获取ZnSO4晶体的实验方案:________________(实验中须使用的试剂有:Zn粉、稀H2SO4、酒精)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com