
科目: 来源: 题型:
【题目】雾霾成因有多种,其中燃煤过程中产生的二氧化硫、氮氧化物以及可吸入颗粒物是山西冬季雾霾的主要组成。治霾迫在眉睫,利在千秋。
I.脱氮
已知: ①2CO(g)+O2(g)===2CO2(g) ΔH1=-566.0 kJ·mol-1
②2NO(g)+O2===2NO2(g) ΔH2=-116.5kJ·mol-1
③N2(g)+O2(g)===2NO(g) ΔH3=+180.5kJ·mol-1
(1)则燃煤所产生的废气中NO2 与CO 转化成无污染气体的热化学方程式为:________________________________。
(2)若1molN2(g)1mo1O2(g)分子中化学键断裂时分别吸收946kJ、498KJ的能量,则1mo1NO(g) 分子中化学键断裂时需要吸收的能量为_____________________KJ。
Ⅱ.脱硫的反应原理2CO(g) +SO2(g)![]() 2CO2(g) +S(1) ΔH=-QkJ·mol-1(Q>0)
2CO2(g) +S(1) ΔH=-QkJ·mol-1(Q>0)
(1)若在一定温度下,将总物质的量为3 mol的CO(g)和SO2(g) 以不同比例充入2 L的恒容容器中,结果如图所示。a、b分别表示SO2、CO的平衡转化率的变化,c表示平衡体系中CO2的体积分数的变化。
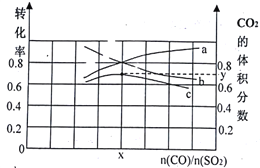
由图计算x=__________;CO2的体积分数y=_________(精确到0.01),该温度下的平衡常数K=_____。
(2)在T1℃下,将CO与SO2按体积比为5∶4充入一恒压密闭容器中,此时容器体积为0.1V L。
①下列能判断该反应达到化学平衡状态的是_____________。
a.S(l)的质量不变
b.K不变
c.容器中气体的平均相对分子质量不变
d.2v正(SO2)= v正(CO2)
e.Q值不变
②压强一定的条件下,在不同温度下进行反应,测得容器的体积变化如图所示:
已知: n1≠n2
温度(℃) | 初始投入总量 | 初始投料v (CO) /v (SO2) | 初始体积(L) | 平衡体积(L) |
T1 | n1 | 5∶4 | 0.1v | 0.07v |
T2 | n2 | 5∶4 | 0.3v | 0.22v |
求:T1温度时,SO2的平衡转化率为_____%;
比较大小,T1___T2(填“>”、“<”、“=”),解释原因____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列涉及化学学科观点的有关说法正确的是![]()
A. 微粒观:二氧化硫是由硫原子和氧原子构成的
B. 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和
C. 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g
D. 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异
查看答案和解析>>
科目: 来源: 题型:
【题目】碳、氧、氯、镁、镍、铜是几种重要的元素,请回答下列问题:
(1)镍元素的核电荷数为28,则基态原子的电子排布式为____________________,结构中有__________种不同形状的电子云。
(2)MgO的熔点高于CuO的理由是________________________________________。
(3)镁原子第一电离能反常地高于铝的原因是_____________________________。
(4)Ni与CO能形成配合物![]() ,该分子中
,该分子中![]() 键与
键与![]() 键个数比为__________。
键个数比为__________。
(5) ![]() 分子中的中心原子杂化轨道类型是__________,该分子的空间构型为__________。
分子中的中心原子杂化轨道类型是__________,该分子的空间构型为__________。
(6)铜与氧可形成如图所示的晶胞结构,其中铜原子均匀地分散在晶胞内部,a、b原子的坐标参数依次为(0,0,0)、![]() ,则d原子的坐标参数为____________________,已知:该晶体的密度为
,则d原子的坐标参数为____________________,已知:该晶体的密度为![]() ,
, ![]() 是阿伏加德罗常数的值,则晶胞参数为__________cm(列出计算式即可)。
是阿伏加德罗常数的值,则晶胞参数为__________cm(列出计算式即可)。

查看答案和解析>>
科目: 来源: 题型:
【题目】芳樟醇和橙花叔醇是决定茶叶花甜香的关键物质。芳樟醇和橙花叔醇的结构如图所示,下列有关叙述正确的是
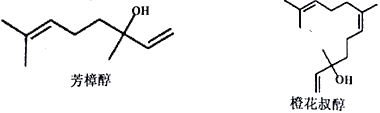
A. 橙花叔醇的分子式为C15H28O
B. 芳樟醇和橙花叔醇互为同分异构体
C. 芳樟醇和橙花叔醇与H2完全加成后的产物互为同系物
D. 二者均能发生取代反应、加成反应、还原反应,但不能发生氧化反应
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列物质的电离方程式:
H2CO3_________________;
NaHCO3_________________;
K2SO4___________________;
NH4NO3__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】中共十九大报告指出,加快水污染防治、实施流域环境和近岸海域综合治理、环境污染的治理是化学工作者研究的重要课题,也是践行“绿水青山就是金山银山”的重要举措。请回答下列问题:
(1)氨氮水体污染可用次氯酸除去,已知:
Ⅰ. ![]()
Ⅱ. ![]()
Ⅲ. ![]()
写出水体中![]() 与
与![]() 反应生成
反应生成![]() 的热化学方程式:____________________________。
的热化学方程式:____________________________。
(2)工业上可用排放的![]() 与
与![]() 合成尿素的方法,达到
合成尿素的方法,达到![]() 减排的目的:
减排的目的: ![]() 。
。
①一定条件下,在1L的密闭容器中充入1mol![]() 和一定量的
和一定量的![]() ,模拟工业生产得到
,模拟工业生产得到![]() 的平衡转化率(
的平衡转化率(![]() )随氨碳比
)随氨碳比 的变化如图所示,其他条件不变,
的变化如图所示,其他条件不变, ![]() 随
随![]() 增大而增大的原因是_______________________________________________;实际工业生产中氨碳比控制在4.0左右,而不是4.5的原因是____________________________________;该温度下反应的平衡常数
增大而增大的原因是_______________________________________________;实际工业生产中氨碳比控制在4.0左右,而不是4.5的原因是____________________________________;该温度下反应的平衡常数![]() ______________________________。
______________________________。

②若![]() ,在1L的恒容密闭容器中充入一定量的
,在1L的恒容密闭容器中充入一定量的![]() 和
和![]() ,此时体系压强为
,此时体系压强为![]() ,5min达到平衡时生成1mol
,5min达到平衡时生成1mol![]() ,此时容器内压强为
,此时容器内压强为![]() ,则用
,则用![]() 表示该反应的平均速率为______________________________,
表示该反应的平均速率为______________________________, ![]() 的平衡转化率为__________。
的平衡转化率为__________。
(3)采用电解法可使酸性废水中的![]() 转经为
转经为![]() 而除去,则阴极的电极反应式为________________________________________。
而除去,则阴极的电极反应式为________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是实验室蒸馏石油的实验装置,实验需要收集60~150℃和150~300℃的馏分。请回答下列问题:
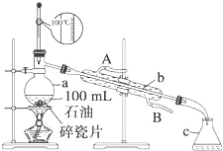
(1)仪器a的规格和名称_______,仪器b、c的名称:b_______,c_______。
(2)实验所选温度计是错误的,正确的选择应该是_______。
(3)实验时在仪器a中加入了少量碎瓷片,其目的是_______。
(4)实验时在仪器b中通入冷却水,请指明冷却水的流向_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】请在标有序号的空白处填空:以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答有关问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是(可多选)__________。
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl→CH3CH2Cl+H2O
C.CH3CH3+Cl2![]() CH3CH2Cl+HCl
CH3CH2Cl+HCl
D.CH2=CHCl+H2![]() CH3CH2Cl
CH3CH2Cl
由上述四个反应可归纳出,原子经济性高的是__________反应(填反应类型)。
(2)有毒物质的无害化也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,还可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性酸根离子氧化除去。请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式________,并说明该方法的优点_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子在溶液中可以大量共存,加入氢氧化钠溶液后也不产生沉淀的是( )
A.Na+、Ba2+、Cl-、SO42-B.K+、Na+、NO3-、OH-
C.H+ 、NH4+、Fe3+、SO42-D.H+、Cl-、CO32-、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com