
科目: 来源: 题型:
【题目】二氧化硫分别通入下表所列溶液(装入试管)中至现象明显,如表实验报告记录的实验现象正确的是( )
石蕊试液 | 品红溶液 | 饱和硫化氢溶液 | 氯水 | |
A | 无色 | 无色 | 乳白色浑浊 | 无色 |
B | 红色 | 无色 | 黄色浑浊 | 无色 |
C | 红色 | 无色 | 乳白色浑浊 | 黄绿色 |
D | 无色 | 无色 | 乳白色浑浊 | 黄绿色 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列 4个图像能正确反映对应变化关系是( )
A | B | C | D |
|
|
|
|
向一定量稀硫酸中加入 NaOH 溶液 | 浓硫酸长期暴露在空气中 | 向一定量的硫酸溶液中逐滴滴入氢氧化钡溶液至过量 | 相同条件下,加热等质量的两份固体,a为氯酸钾和二氧化锰的混合物,b 为氯酸钾 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验中,对应的现象以及结论都正确且两者相符的是( )
选项 | A | B | C | D |
实 验 |
|
|
|
|
实 验 现 象 | 打开汽水瓶盖时,汽水 会自动喷出来 | 碘溶于水,几乎不溶于 汽油 | 白磷燃烧,产生大量白烟,活塞先向右再向左移,冷却至室温后,最终停在刻度“4”附近 | 空气中,带火星的木条复燃;呼出气体中,带火星的木条熄灭 |
实 验 结 论 | 说明气体在水中的溶解度随压强的增大而减小 | 说明物质的溶解性与溶剂的种类有关 | 氧气约占空气体积的五分之一 | 空气中的氧气比呼出气体中氧气多 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】甲乙是某同学设计的两套制取二氧化碳的发生装置,对两套装置分析正确的是

A. 此时甲装置中的止水夹M处于打开状态
B. 甲装置气体导出过程中容器内外气压相等
C. 甲装置不具有启普发生器的功能
D. 乙装置N处添加止水夹可以与甲装置具有相同功能
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25℃、101kPa时,一些物质的燃烧热为,回答下列问题:
化学式 | CO(g) | H2(g) | CH3OH(l) | CH4(g) |
△H/(kJ·mol-l) | -283.0 | -285.8 | -726.5 | -890.3 |
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:_____________________________。
(2)根据盖斯定律完成下列反应的热化学方程式:CO(g)+2H2(g)![]() CH3OH(l)△H=__________。
CH3OH(l)△H=__________。
(3)工业上利用水煤气合成甲醇的主要反应可表示为![]() CO(g)+H2(g)
CO(g)+H2(g)![]()
![]() CH3OH(g)△H=-45.4kJ·mol-1。向容积为1L的密闭容器中加入0.10molH2和0.05molCO,在一定温度下发生上述反应,10min后反应达到平衡状态,测得放出热量3.632kJ。
CH3OH(g)△H=-45.4kJ·mol-1。向容积为1L的密闭容器中加入0.10molH2和0.05molCO,在一定温度下发生上述反应,10min后反应达到平衡状态,测得放出热量3.632kJ。
①相同温度条件下,上述反应的化学平衡常数K=___________。
②若容器容积不变,下列措施可增加CH3OH产率的是___________ (填标号)。
a.升高温度
b.将CH3OH(g)从体系中分离
c.充入He,使体系总压强增大
d.再充入0.10molH2和0.05molCO
e.加入催化剂
③反应达到平衡后,保持其他条件不变,若只把容器的体积缩小一半,平衡将___________(填“逆向”“正向”或“不”)移动,化学平衡常数K___________(填“增大”“减小”或“不变”)。
④温度、容积相同的甲、乙两个密闭容器,若甲中加入1molCO和2molH2,乙中加入lmolCH3OH(g),反应达到平衡时甲放出的热量为Q1kJ,乙吸收的热量为Q2kJ,甲中CO的转化率为a1,乙中CH3OH的转化率为a2,则Q1+Q2=___________,a1+a2=___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】人尿中可以分离出具有生长素效应的化学物质——吲哚乙酸,吲哚乙酸的结构如下图所示。
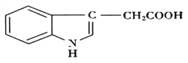
下列有关说法正确的是
A. 吲哚乙酸与苯丙氢酸互为同系物
B. 吲哚乙酸苯环上的二氯代物共有四种
C. 1mol吲哚乙酸与足量氢气发生反应,最多消耗5molH2
D. 吲哚乙酸可以发生取代反应、氧化反应和还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式碳酸镁可用于牙膏、医药化妆品等工业,化学式为4MgCO3·Mg(OH)2·5H2O,某碱式碳酸镁中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下两个方案:
方案I:
取一定质量的样品,与硫酸充分反应,通过测定CO2的质量计算纯度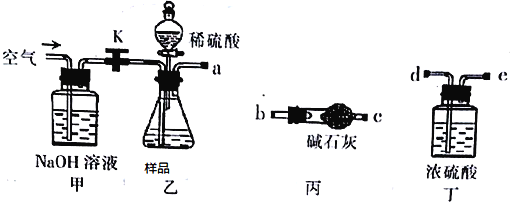
(1)乙中发生反应的方程式为______________________________ 。
(2)仪器接口的连接顺序为(装置可以重复使用) a__________,丁的作用是_________。
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是______________________________。
方案Ⅱ:
①称取碱式碳酸镁样品mg;②将样品充分高温灼烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用托盘天平称量)。
(4)下列仪器中,该方案不会用到的是____________。
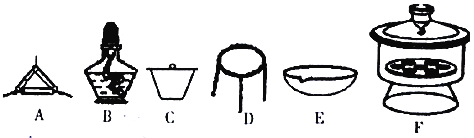
(5)有同学认为方案Ⅱ高温灼烧的过程中会发生MgCO3+SiO2![]() MgSiO3+CO2↑会导致测定结果有误,你认为这位同学的观点是否正确_____,(填“正确”或“错误”)请说明自己的理由:______________________。
MgSiO3+CO2↑会导致测定结果有误,你认为这位同学的观点是否正确_____,(填“正确”或“错误”)请说明自己的理由:______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】分类是学习和研究化学物质及其变化的一种常用的科学方法。
(1)下列4组物质中均有一种物质的主要化学性质与其他3种不同。
A.CaO、Na2O、CO2、MgO B.CH3COOH、H2SO4、Ba(OH)2、HNO3
C.H2、Cl2、P、Cu D.HCl、CH3CH2OH、H2SO3、HNO3
①写出D组中不同于其他三种的物质的化学式:______________。
②A组中的一种物质与B组中的一种物质反应,反应物的量不同产物有所不同。写出这两种物质反应有沉淀产生的离子反应方程式:____________________________。
③C组中Cu在一定条件下可与H2、Cl2、P反应生成CuH、CuCl2、Cu3P等化合物。写出CuH在Cl2中燃烧的化学方程式:___________________________________。
(2)NaOH、Na2CO3、NaAlO2溶液都具有碱性。向500mL由NaOH、Na2CO3、NaAlO2组成的混合溶液中滴加0.2mol·L-1盐酸,所消耗盐酸体积如图所示,回答下列问题:

①写出加盐酸V1至V2段反应的离子方程式:_______________________________。
②用36.5%(密度为1.19g·mL-1)的浓盐酸配制945mL0.2mol·L-1盐酸,需要量取的浓盐酸体积为___________________。
③若V1=50mL,V2=100mL,V3=200mL,则V4=___________。原混合溶液中NaOH、Na2CO3、NaAlO2的物质的量之比为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体。下图表示反应中的各种分子,其中不同的球表示不同种元素的原子。下列说法中,不正确的是 ( )
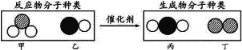
A. 乙、丙所含元素种类相同 B. 甲、丁中同种元素化合价不相等
C. 该反应中共有三种元素 D. 化学方程式中乙、丁的化学计量数均为1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com