
科目: 来源: 题型:
【题目】常温下,向20.00mL 0.200 0 mol/LNH4Cl溶液中逐滴加入0.2000 mol/LNaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。下列说法正确的是
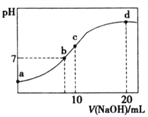
A. a点溶液中:c(H+)+c(NH3·H2O)=c(OH-)+c(NH4+)
B. b点溶液中:c(Cl-)=c(Na+)>c(H+)=c(OH-)
C. c点溶液中:c(NH3·H2O)+ c(NH4+)= c(Cl-)+ c(OH-)
D. d点溶液中:c(Cl-)> c(NH3·H2O)> c(OH-)> c(NH4+)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知锌及其化合物的性质与铝及其化合物相似。如图横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4 ]2-的物质的量浓度的对数。25℃时,下列说法中不正确的是
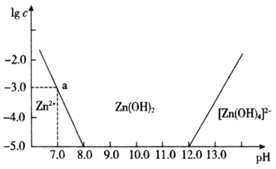
A. 往ZnCl2溶液中加入过量氢氧化钠溶液,反应的离子方程式为Zn2++4OH-=[Zn(OH)4]2-
B. 若要从某废液中完全沉淀Zn2+,通常可以调控该溶液的pH在8.0—12.0之间
C. pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108
D. 该温度时,Zn(OH)2的溶度积常数(Ksp)为1×l0-10
查看答案和解析>>
科目: 来源: 题型:
【题目】下图一所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液,足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。

(1)图一中的直流电源为一种性能优良的Al-Ag2O电池,其原理如图二所示。该电池中铝是负极,试写出电池工作时的正极反应式__________________和电池的总化学反应方程式______________。
(2)接通电源后,经过一段时间后,测得丙中K2SO4质量分数为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为_______极;c电极上发生______反应(“氧化”或“还原”);
②电极b上发生的电极反应为___________________;
③列式计算电极b上生产的气体在标准状况下的体积_______;
④电极c的质量变化是_____g;
⑤电解前后各溶液的pH是否发生变化(“增大”、“减小”或“不变”)
甲溶液_________;乙溶液_________;丙溶液______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铜(CuCl)是一种白色粉末,不溶于水、乙醇(标准状况下沸点是78.2℃)及稀硫酸,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用于有机合成工业中的催化剂。以粗盐水(含氯化钙、硫酸镁等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如下:
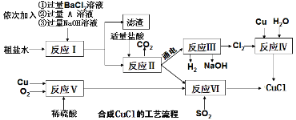
(1)A溶液中溶质的化学式是__________ ;
(2)写出反应V的化学方程式 _______________ ;
(3)反应VI的化学方程式是:2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4,反应中化合价升高的元素是___;
(4)本工艺中可循环利用的物质是NaOH和_____;
(5)反应VI后,过滤得到的CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却密封包装即得产品。真空干燥的目的是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等。下列叙述中不正确的是( )

A.三种元素的原子半径的大小顺序是W<Y<X
B.W最高价氧化物对应水化物具有强酸性,气态氢化物的水溶液具有弱碱性
C.X元素的氧化物、氢化物的水溶液都呈酸性
D.Y元素的单质是非金属单质中唯一能跟水发生激烈反应的单质
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关元素周期表的说法正确的是( )
A.元素周期表有7个周期,8个主族
B.零族原子的最外层电子数均为8
C.同一主族元素,最外层电子数一定相同
D.短周期是指第1、2、3、4周期
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )。
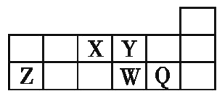
A.Y原子的电子总数是其K层电子数的3倍
B.原子半径大小顺序为r(X)>r(Y)>r(Z)>r(W)>r(Q)
C.Q的单质能与W的氢化物发生置换反应
D.元素W的最高价氧化物对应水化物的酸性比Q的强
查看答案和解析>>
科目: 来源: 题型:
【题目】可以用离子方程式2H++CO32﹣=H2O+CO2↑来表示的化学反应是( )
A.硝酸和碳酸氢钠溶液的反应
B.稀硫酸和碳酸钾溶液的反应
C.醋酸和碳酸钠溶液的反应
D.盐酸和碳酸钡溶液的反应
查看答案和解析>>
科目: 来源: 题型:
【题目】美国华裔科学家叶军领导一个研究小组成功制造出全球最准确的时钟,两亿年误差不足一秒。它是一个锶原子钟,比铯原子喷泉钟准确得多,估计将可大大促进不同的电讯网络的发展,将使全球各地的船只导航变得更为准确。请根据锶、铯在元素周期表中的位置,推断下列内容:
(1)锶元素属于________(填“金属”或“非金属”)元素,金属性比钙元素________(填“强”或“弱”),锶原子的核内质子数为________,原子核外有________个电子层,其原子结构示意图为:___________,其原子半径___________镁(填“大于”、“小于”或“等于”);铯的原子核外共有________层电子,最外层电子数为___________。
(2)铯与水起剧烈反应,放出___________色气体,同时使滴有紫色石蕊试液的溶液显___________色,因为___________(写出化学方程式)。
(3)碳酸锶是________色粉末,与盐酸反应的离子方程式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是周期表中的一部分,根据A~I在周期表中位置,用元素符号或化学式回答下列问题:

(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的是________,氧化性最强的单质是________,还原性最强的单质是________。
(2)元素的最高价氧化物对应的水化物中,碱性最强的是________,酸性最强的是________,呈两性的是________。
(3)A分别与D、E、F、G、H形成的化合物的分子式分别为________,最稳定的是________。
(4)在B、C、D、E、F、G、H中,原子半径最大的_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com