
科目: 来源: 题型:
【题目】下图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是( )
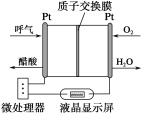
A.该电池的负极反应式为CH3CH2OH+3H2O-12e-===2CO2↑+12H+
B.该电池的正极反应式为O2+4e-+4H+===2H2O
C.电流由O2所在的铂电极经外电路流向另一电极
D.微处理器通过检测电流大小而计算出被测气体中酒精的含量
查看答案和解析>>
科目: 来源: 题型:
【题目】镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运等特点。研究的燃料电池可分为镁—空气燃料电池,镁—海水燃料电池,镁—过氧化氢燃料电池,镁—次氯酸盐燃料电池。如图为镁—次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )
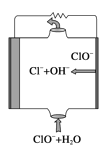
A.放电过程中OH-移向正极
B.电池的总反应式为Mg+ClO-+H2O===Mg(OH)2↓+Cl-
C.镁电池中镁均为负极,发生氧化反应
D.镁—过氧化氢燃料电池,酸性电解质中正极反应式为H2O2+2H++2e-===2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是( )。

A.正极反应式:Ca+2Cl--2e-=CaCl2
B.放电过程中,Li+向负极移动
C.每转移0.1 mol电子,理论上生成20.7 g Pb
D.常温时,在正、负极间接上电流表或检流计,指针不偏转
查看答案和解析>>
科目: 来源: 题型:
【题目】阿司匹林是一种历史悠久的解热镇痛药,对预防血栓和脑梗有很好的作用,M是一种防晒剂,它们的结构简式分别为
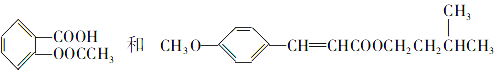 ,
,
它们的合成路线如下:

已知:Ⅰ. E的俗称水杨酸,学名2-羟基苯甲酸

IV.苯的同系物与氯气的反应遵循“催化在苯环,光照在侧链”。
根据以上信息回答下列问题
(1)阿司匹林中官能团的名称为______
(2) B→D过程的反应类型为______请写出C和I的结构简式________________
(3)由E→F的过程是缩聚反应,该过程化学方程式为_________
(4)下列关于阿司匹林和防晒剂M说法正确的是_________(双选)
A.M的分子式是C15H20O3
B.其中阿司匹林不能发生氧化反应
C.1mol阿司匹林完全水解,需消耗2molNaOH
D.1molM与足量氢气发生加成反应,最多消耗4molH2
(5)阿司匹林有多种同分异构体,请写出同时满足下列条件的任意一种同分异构体的结构简式________
ⅰ.苯环上有2个取代基;
ⅱ.能发生水解反应,能发生银镜反应,还能与NaHCO3产生CO2
iii.核磁共振氢谱有5组峰,峰面积之比为1:1:2:2:2
(6)写出由I到M的合成路线(第一步已给出):合成路线示例如下:
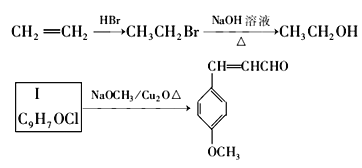 __________________________
__________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________;K、F、Zn的电负性从大到小的顺序为___________。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________。
(3)OF2分子的几何构型为___________(1分),中心原子的杂化类型为___________。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3中除σ键外,还存在___________。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为___________个。
②该晶体的密度为___________(列出算式即可,用NA表示阿伏加德罗常数的数值)g·cm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4===2PbSO4+2H2O。
正极电极反应式为______________。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu===2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为_____________,当线路中转移0.2 mol电子时,则被腐蚀铜的质量为_____________g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为______________。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的总反应化学方程式是:________________。
②电池工作一段时间后硫酸溶液的浓度_____________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一包白色粉末可能含硫酸钡、碳酸钠、和氢氧化钡中的一种或几种,取一定量的该粉末加入到盛有足量水的烧杯中,搅拌、静置,观察到有白色不溶物。
小张同学认为,白色粉末中一定含有硫酸钡;
小李同学认为,小张同学的结论不准确,其理由可用化学方程式表示为______________。
针对上述两名同学的观点,小刘同学进一步设计如下实验方案进行探究:

(1)步骤③中,滴入酚酞溶液后,若滤液E为红色,则滤液E中除酚酞外还一定含有的溶质是_______(填化学式,下同),由此得出原白色粉末成分组成的结论是______________。
(2)小王同学认为,只需要取少量滤渣B,加入过量的稀盐酸,若看到的现象是白色不溶物部分溶解,且有气泡产生,就足以说明原白色粉末的成分是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种重要的化工原料,工业上可用CO和H2合成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) ![]() CH3OH(g) ΔH = -90.8 kJ·mol-1
CH3OH(g) ΔH = -90.8 kJ·mol-1
(1)某研究小组,在温度和容器的容积保持不变时,研究该反应是否达到平衡状态,以下五位同学对平衡状态的描述正确的是__________。
A.甲:H2的消耗速率等于CH3OH的生成速率
B.乙:容器内的压强保持不变
C.丙:容器内气体的密度保持不变
D.丁:容器中气体的平均摩尔质量保持不变
(2)若在一定温度下、容积为2L的密闭容器中,投入2 mol CO、4 mol H2,保持恒温、恒容,测得反应达到平衡时H2转化率为75%,求平衡时CH3OH的浓度=__________mol/L
(3)已知在298K、101kPa下:甲醇的燃烧热化学方程式为:
CH3OH(l)+ 3/2 O2(g)= CO2(g)+ 2H2O(l) ΔH= -725.8 kJ·mol-1;
CO的燃烧热化学方程式为:CO(g)+ 1/2 O2(g)= CO2(g) ΔH= -283 kJ·mol-1;
H2O (g) === H2O(l) ΔH= -44 kJ·mol-1
请写出甲醇不完全燃烧生成一氧化碳和水蒸气的热化学方程式__________。
(4)以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)
①该电池中通入甲醇的是电源的__________(填正、负)极,若KOH溶液足量,则写出电池总反应的离子方程式__________。
②若电解质溶液中KOH的物质的量为0.5mol,当有0.5mol甲醇参与反应时,产物恰好为KHCO3时,该电池的负极反应式为__________,所得溶液中各种离子的物质的量浓度由大到小的顺序是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案,请完成有关问题。
方案Ⅰ:将形状和大小均相同的铁片和铜片,分别同时放入100 mL 2.0 mol·L-1稀硫酸中,观察反应的情况,据此确定它们的金属活动性。
方案Ⅱ:利用Fe、Cu作电极设计成原电池,以确定它们的金属活动性。
(1)方案Ⅰ中发生反应的离子方程式为 。
(2)在方框内画出方案Ⅱ中的原电池装置图,注明电解质溶液名称和正、负极材料,标出电子流动方向,并写出电极反应式:
正极: ;
负极: 。
(3)结合你所学的知识,请你再设计一个与方案Ⅰ、Ⅱ不同的验证Fe、Cu活动性的简单实验方案: ,用离子方程式表示其反应原理: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com