
科目: 来源: 题型:
【题目】铬及其化合物在工业生产中有重要的用途。
(1)向Na2CrO4溶液中加入稀硫酸酸化,会生成Na2Cr2O7(重铬酸钠),酸化过程中发生反应的离子方程式为______________。不能选用盐酸进行酸化的原因是______________。
(2)重铬酸钾(K2Cr2O7)可用于检验酒驾,其原理是人呼出的乙醇会使硫酸酸化的重铬酸钾硅胶变为灰绿色的硫酸铬[Cr2(SO4)3],乙醇被氧化成乙酸,写出反应的离子方程式:______________。
(3)已知常温下Ksp[Cr(OH)3]=6.0×10-31,在Cr2(SO4)3溶液中滴加NaOH溶液调节至溶液中c(Cr3+)=6.0×10-16 mol/L时,溶液的pH=______________。
(4)用氧化还原滴定法可测定废水中Cr2O72-的浓度。取100 mL废水样品,加入少许稀硫酸和过量的KI溶液,充分反应后滴入几滴淀粉溶液,用0.2 mol/L的Na2S2O3溶液滴定生成的I2,当滴入30 mL Na2S2O3溶液时恰好反应完全,反应的原理是Cr2O72-+14H++6I- =3I2 +2Cr3++7H2O;I2 +2S2O32- =2I- +S4O62-,则该废水中Cr2O72-的物质的量浓度是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向1L0.1mol·L-1一元酸HR溶液中逐渐通入氨气[已知常温下Kb(NH3·H2O)=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如下图所示。下列叙述正确的是( )

A. 0.1mol·L-1HR溶液的pH约为5 B. HR为弱酸,常温时Ka(HR)=1.0×10-7
C. 当通入0.1molNH3时,溶液中c(R-)<c(NH4+) D. 当c(HR)=c(R-)时,溶液呈中性
查看答案和解析>>
科目: 来源: 题型:
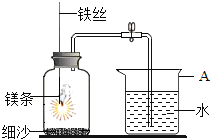
【题目】某学习小组用右图做镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%。
(1)瓶底铺细沙的原因是__________________________________________;
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的________%。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成推测原因可能是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素X、Y、Z、R、T的原子半径与原子序数的关系如图所示。Y与Z能形成Z2Y、Z2Y2型离子化合物R原子最外层电子数是电子层数的2倍,Z与T形成的化合物Z2T能破坏水的电离平衡。下列说法正确的是

A. 简单氢化物的热稳定性:R>Y
B. 简单离子的半径:Y>Z
C. 最高价氧化物对应水化物的酸性:R>T
D. Y与T属于同一主族、与X属于同一周期
查看答案和解析>>
科目: 来源: 题型:
【题目】稀有金属钌(Ru)的性质很稳定,耐腐蚀。实验室用H2还原RuO2来制备金属钌的装置如图所示。下列说法错误的是
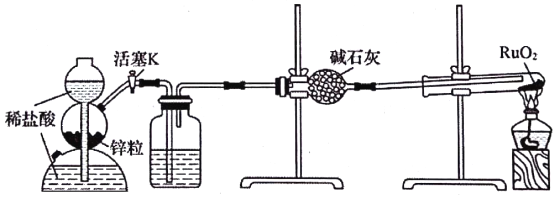
A. 加热RuO2前,应先收集气体并点燃,通过声音判断气体纯度
B. 洗气瓶中盛装的可能是NaOH溶液,用于除去挥发出来的HCl气体
C. 结束反应时,先停止加热,待试管冷却到室温后再关闭活塞K
D. 启普发生器也可用于碳酸钠晶体与稀硫酸反应制备二氧化碳
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E五种元素的原子序数依次增大,A元素位于周期表的s区,其原子中电子层数等于未成对电子数;B的基态原子中电子占据三种能量不同的原子轨道,且每种原子轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体;A、B两种元素组成的原子个数之比为1∶1的化合物N是常见的有机溶剂;E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
(1)E的基态原子的价电子排布图为______。
(2)B、C、D三种元素的氢化物的沸点高低顺序为__________(用化学式表示,下同),稳定性顺序为__________。
(3)化合物M是同类物质中为数不多的气体,且分子中所有原子共平面,则M中σ键和π键个数比为____,B原子的杂化类型为____,M能和水以任意比混溶的原因是______________。
(4)E的一种氧化物Q,其晶胞结构如图1所示,则Q的化学式为____。

(5)电镀厂排放的废水中常含有剧毒的BC-,可在Q的催化下,先用NaClO将BC-氧化成BCD-,然后在酸性条件下BCD-可以继续被NaClO氧化成C2和BD2。
①与BCD-互为等电子体的分子是____(写出一种即可);可以推知BCD-的空间构型为__。
②上述反应中后一步反应的离子方程式为_____________。
(6)E内部原子的堆积方式与铜相同,都是面心立方堆积方式,如图2所示,则E晶胞中E的配位数为____,若该晶胞的密度为a g·cm-3,阿伏加德罗常数为NA,E原子的摩尔质量为M g·mol-1,则E原子的半径为____cm。
查看答案和解析>>
科目: 来源: 题型:
【题目】某市中考化学实验操作考试有四个考题:①蒸馏;②H2的化学性质;③二氧化碳的制取、收集和验满;④氧气的制取、收集和验满。考试的方法是由考生抽签确定考题,小凯同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:

请回答:
(1)指出上图中仪器a的名称:_______;
(2)由实验台上提供的仪器和药品,你认为小凯抽到的是第____个考题;
(3)以下是小凯完成该实验主要操作过程的示意图。按评分标准,每项操作正确得1分,满分5分,实验完毕后小凯得了3分。请找出他失分的操作并说明原因:______________________、______________________;
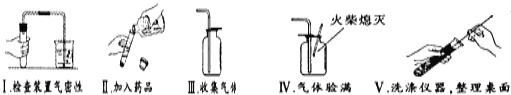
(4)仅用上述仪器(药品另选),也能完成另一种常见气体的实验室制取,化学方程式为:______________;若增加________ (填一种玻璃仪器名称)还能组装成高锰酸钾制氧气的发生装置。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据学过的化学知识填空:
(1)金刚石和石墨物理性质差异较大的原因是____________________;一氧化碳和二氧化碳性质不同的原因是_____________________。
(2)天然气的主要成分燃烧的化学方程式是_________________________。
(3)煤在空气中燃烧需要满足的条件是__________;吹灭蜡烛的原理是____________。
(4)生铁和钢都是铁的合金,由于________不同,二者性能不同。
查看答案和解析>>
科目: 来源: 题型:
【题目】将下列各组物质按单质、酸、碱、盐分类顺序排列,其中正确的是( )
A.水银、硫酸、烧碱、硫酸氢钠
B.氯水、盐酸、火碱、硫酸钡
C.臭氧、硝酸、纯碱、胆矾
D.铜、醋酸、石灰石、氯化铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com