
科目: 来源: 题型:
【题目】实现下列变化时,需克服相同类型作用力的是( )
A. 二氧化硅和干冰的熔化 B. 食盐和葡萄糖分别溶解在水中
C. 锌和氯化铵的熔化 D. 液氯和苯的汽化
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,下列叙述不能作为可逆反应A(g)+3B(g)![]() 2C(g)达到平衡标志的是
2C(g)达到平衡标志的是
①C的生成速率与C的消耗速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④C的物质的量不再变化
⑤混合气体的总压强不再变化
⑥混合气体的总物质的量不再变化
⑦单位时间消耗a molA,同时生成3a mol B
⑧A、B、C的分子数之比为1:3:2
A. ⑤⑥B. ⑦④C. ①③D. ②⑧
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在一定容积的密闭容器中加入NH3和O2各1mol,发生反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)。下列说法中,表明该反应达到化学平衡状态的是
4NO(g)+6H2O(g)。下列说法中,表明该反应达到化学平衡状态的是
A. 反应速率不再变化 B. NH3和NO的反应速率相等
C. 气体的密度不再变化 D. NO和H2O浓度比不再变化
查看答案和解析>>
科目: 来源: 题型:
【题目】汽车尾气主要含有CO2 、CO、SO2、NOx 等物质,尾气中CO、氢氧化物(NOx) 严重影响人们的生活和健康,化学工作者对氮氧化物的处理做了广泛而深入的研究。
(1)利用甲烷还原NOx
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mo l;
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+H2O(g) △H2=-1160kJ/mo l,
甲烷直接将NO2还原为N2的热化学方程式为________________________________。
(2)将不同量的CO(g)积H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 4 |
3 | 900 | a | b | c | d | t |
①实验1中以v(CO2) 表示的反应速率为/span>_________(保留两位有效数字,下同)。
②该反应为________(填“吸热”或“放热”) 反应,实验2条件下的平衡常数K=________。
③若达平衡状态时,实验2 与实验3中各物质的质量分数分别相等,且t<4min,则a、b应满足的关系是_________________________(用含a、b的数学式表示)。
(3)CO分析仪的传感器可测定汽车尾气是否符合排放标准。该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3) 和氧化锆(ZrO2) 晶体,能传导O2-,则负极的电极反应式为____________。
(4)SO2可用钙基固硫反应除去,反应生成的CaSO4是一种微溶物质,其Ksp=9.0×10-6。若将浓度为2×10-3mol/L的Na2SO4溶液与等体积的CaCl2溶液混合,则生成沉淀所需CaCl2溶液的最小浓度为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、W、Q四种元素在元素周期表中的位置如图,下列叙述错误的是

A. Y的氢化物沸点高于Q的氢化物沸点
B. 原子半径顺序为:r(W)>r(Q)>r(Y)>r(X)
C. 最高正价与最低负价之和为0的元素只有W
D. X、Y、Q三元素形成的分子中,原子最外层电子数之和最大为32
查看答案和解析>>
科目: 来源: 题型:
【题目】在合成氨反应中,将等物质的量的氮气和氢气充入一密闭容器中发生反应,测得 2min 内氨的平均反应速率为 2 mol·L-1·min -1,2min 末 N2 的浓度为7 mol·L-1,则氢气的起始浓度为
A.9 mol·L-1
B.6 mol·L-1
C.3 mol·L-1
D.2 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】氟碳铈矿的主要化学成分为CeFCO3,它是提取铈族稀土元素的重要矿物原料,二氧化铈(CeO2) 是一种重要的稀土氧化物。以氟碳铈矿为原料制备CeO2的一种工艺流程如下:
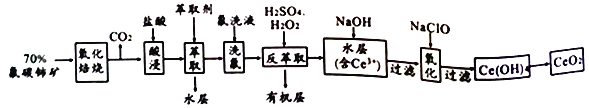
已知:①Ce 4+既能与F 结合成[CeFx](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+ 能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1) “氧化焙烧”的目的是______________。
(2)“酸浸”中会产生大量黄绿色气体、请写出CeO2与盐酸反应的离子方程式___________________;为避免产生上述污染,请提出一种解决方案________________________。
(3)“萃取”时存在反应:Ce4++n(HA)2![]() Ce+(H2a-4A2a)+4H+。实验室中萃取时用到的主要玻璃仪器为______________;若缺少 “洗氟”,则所得产品的质量将_________(填“偏大”、“偏小”或 “不变”)。
Ce+(H2a-4A2a)+4H+。实验室中萃取时用到的主要玻璃仪器为______________;若缺少 “洗氟”,则所得产品的质量将_________(填“偏大”、“偏小”或 “不变”)。
(4) “反萃取”中,加稀硫酸和H2O2的作用__________________(用离子方程式表示)。
(5)取上述流程中得到的CeO2产品0.500g,加硫酸溶解后,用0.1000mol·L-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其它杂质均不参加反应)消25.00mL标准溶液,该产品中CeO2的质量分数为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】合成金刚石的新方法化学原理为:①Na+CO2![]() C(金刚石)+C(石墨)+Na2CO3(未配平);方法比人工首次制得金刚石的旧方法:②C(石墨)=C(金刚石)容易得多。以下表述中正确的是
C(金刚石)+C(石墨)+Na2CO3(未配平);方法比人工首次制得金刚石的旧方法:②C(石墨)=C(金刚石)容易得多。以下表述中正确的是
A. 反应②中既有旧化学键的断裂又有新化学键的形成
B. 新方法利用的是化学变化,旧方法利用的是物理变化
C. 在反应①中每生成12 g金刚石需要消耗46 g金属钠
D. 反应①和反应②中所得的金刚石都是还原产物
查看答案和解析>>
科目: 来源: 题型:
【题目】对于化学反应C(s)+O2(g)=CO2(g)来说,下列有关说法正确的是( )
A. 增加固体碳的物质的量,化学反应速率会加快
B. 升高温度,化学反应速率会加快
C. 升高温度,化学反应速率会变慢
D. 升高温度,固体碳能充分燃烧
查看答案和解析>>
科目: 来源: 题型:
【题目】下列仪器:①烧杯、②坩埚、③锥形瓶、④蒸发皿、⑤试管、⑥烧瓶、⑦表面皿,用酒精灯加热时,需要垫石棉网的是( )
A.②④⑤
B.①⑥⑦
C.③④⑥
D.①③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com