
科目: 来源: 题型:
【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.3 | 7.6 | 4.4 |
完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是_________________。
(2)向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的离子方程式____________________。
(3)为保证产品的纯度,调节pH的范围为___________,调pH值可以选用(填字母)_______。
a.Cu(OH)2 b.H2SO4 c.NH3H2O d.Na2CO3 e.CuO
(4)煮沸硫酸铜溶液的原因是____________。
(5)CuCl产品中CuCI的质量分数大于96.50%为国家合格标准。称取所制备的CuCl样品0.2500g置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol/L的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液24.80mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。则CuCl产品中CuCl的质量分数为_____。
(6)已知Fe(OH)3能与次氯酸钾碱性溶液发生反应生成具有强氧化性的高铁酸钾(K2FeO4),高铁酸钾可作为新型多功能水处理剂的原因是___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是

A. 加入Na2SO4可使溶液由a点变到b点
B. 通过蒸发可以使溶液由d点变到c点
C. d点无BaSO4沉淀生成
D. a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于元素周期表的说法中正确的是
A.同一主族元素的原子序数的差不可能为10
B.同周期第ⅡA族与第ⅢA族元素的原子序数差值一定是1
C.催化剂一般在金属与非金属的分界线处寻找
D.过渡元素全部是金属元素
查看答案和解析>>
科目: 来源: 题型:
【题目】以下关于元素周期表结构的叙述正确的是
A.元素周期表有7个主族,8个副族
B.元素周期表有4个长周期、3个短周期
C.第ⅢA族位于元素周期表的第3列(从左往右)
D.0族位于元素周期表的第16列(从左往右)
查看答案和解析>>
科目: 来源: 题型:
【题目】关于0.1 mol/L醋酸钠溶液,下列说法正确的是
A. 加少量水稀释时,![]() 增大
增大
B. 向其中再加入少量醋酸钠晶体时,溶液中所有离子浓度都增大
C. 离子浓度大小比较:c(CH3COO-) >c(Na+) >c(OH-) > c(H+)
D. 向其中加入盐酸至恰好呈中性时,c(Na+) = c(CH3COO-)
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。A中反应方程式是___________________________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂 :______________________________
③C中得到紫色固体和溶液。C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH![]() 2K2FeO4+6KCl+8H2O,另外还有____________________________________(写离子方程式)。
2K2FeO4+6KCl+8H2O,另外还有____________________________________(写离子方程式)。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
i.由方案Ⅰ中溶液变红可知a中含有_______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由__________________________________________产生(用方程式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________________________。
②根据K2FeO4的制备实验得出:氧化性Cl2_______FeO42-(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验中没有颜色变化的是 ( )
A.葡萄糖溶液与新制的Cu(OH)2悬浊液混合加热B.纸张上涂抹浓硫酸
C.淀粉溶液中加入碘酒D.淀粉溶液中加入稀硫酸
查看答案和解析>>
科目: 来源: 题型:
【题目】某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):

已知:(a) 
(b) ![]() (苯胺易被氧化)
(苯胺易被氧化)
请回答下列问题:
(1)D的结构简式为____;烃A的分子式为________。
(2)反应②的反应类型是__________。
(3)①下列对该抗结肠炎药物有效成分可能具有的性质推测正确的是_______;
A.水溶性比苯酚好 B.能发生消去反应,也能发生聚合反应
C.既有酸性又有碱性 D.1mol该物质最多可与4molH2发生反应
②E与足量NaOH溶液反应的化学方程式为_______________。
(4)符合下列条件的抗结肠炎药物有效成分的同分异构体有____种。
A.遇FeCl3溶液发生显色反应
B.分子中甲基与苯环直接相连
C.苯环上共有三个取代基
(5)已知:苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位,据此按先后顺序写出以A为原料合成邻氨基苯甲酸 (![]() )合成路线中两种中间产物的结构简式(部分反应条件已略去)。A→________→_________→
)合成路线中两种中间产物的结构简式(部分反应条件已略去)。A→________→_________→![]() ____________
____________
查看答案和解析>>
科目: 来源: 题型:
【题目】用标准盐酸滴定未知浓度的氨水溶液(锥形瓶中)时,下列说法正确的是
A. 量取一定体积的氨水用如右图所示仪器![]()
B. 从测定结果的准确性考虑,选择酚酞作指示剂比选甲基橙要好
C. 滴定前滴定管的尖嘴处有气泡,而在滴定后气泡消失,则测定氨水的浓度偏高
D. 滴定过程中,往锥形瓶中加入少量蒸馏水会导致测定的浓度偏小
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,平衡pH随溶液体积变化的曲线如图所示。据图判断正确的是
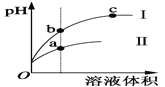
A. Ⅱ为盐酸稀释时pH变化曲线
B. b点溶液的导电性比c点溶液的导电性弱
C. a点KW的值比c点KW的值大
D. 与相同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积,a点比b点大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com