
科目: 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式为C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1∶2∶2∶3,A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A的下列说法中,正确的是( )

A. 1molA在碱性条件下水解消耗2molNaOH
B. A在一定条件下可与4molH2发生加成反应
C. 符合题中A分子结构特征的有机物只有1种
D. 与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列有关叙述正确的是( )
A. 100g质量分数为46%的酒精溶液中含氧原子总数为4NA
B. 电解精炼铜,当外电路转移NA 个电子时,阳极质量减少32g
C. 1L0.1mol·L-1CH3COOH溶液中含H+的数目为0.1NA
D. 常温下,将1molFe加入足量硝酸中,生成H2的分子数为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知: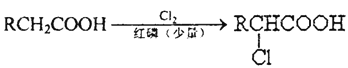
![]()
冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下:
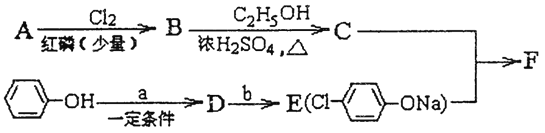
(1)A为一元羧酸,8.8gA与足量NaHCO3溶液反应生成2.24LCO2(标准状况),A的分子式为_________。
(2)写出符合A分子式的所有甲酸酯的结构简式:____________。
(3)B是氯代羧酸,其核磁共振氢谱有两个峰,写出B→C的反应方程式:_______。
(4)C+E→F的反应类型为___________。
(5)写出A和F的结构简式:A______;F_______
(6)D的苯环上有两种氢,它所含官能团的名称为________;写出a、b所代表的试剂:a. _______b. _______。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2 向处理过的铁屑中加入过量的3mol·L-1H2SO4溶液,在 60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3 向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有__________(填仪器编号)
①铁架台 ②燃烧匙 ③锥形瓶 ④广口瓶 ⑤研体 ⑥玻璃棒 ⑦酒精灯
(2)在步骤2中所加的硫酸必须过量,其原因是_______;
(3)在步骤3中,“一系列操作”依次为______、_______和过滤;
(4)本实验制得的硫酸亚铁铵晶体常含有Fe3+杂质。检验Fe3+常用的试剂是______,可以观察到的现象是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】从科学的角度来看,下列说法正确的是( )
A.冬天用煤炉取暖,为防止热量散失,应关紧门窗
B.进入古井前,应先做灯火试验
C.一次性塑料袋使用方便又经济,应大力提倡生产
D.油锅不慎着火,应立即用大量的水冲灭
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钠在氯气中产生________色的烟,反应的化学方程式为_____________________,生成物氯化钠中的化学键是__________键,该化合物是_________(填“离子”、“共价”)化合物,氯化钠的电子式为_____________。氢气在氯气中燃烧产生______色的火焰,反应的化学方程式为_______,氯化氢分子中的化学键是_______键,该化合物是________(填“离子”、“共价”)化合物,氯化氢分子的电子式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】第四周期过渡元素常与H2O、NH3等形成配合物。
(1)写出Fe元素基态原子的价层电子排布式_______;
(2)C、N、O元素的第一电离能从大到小的顺序为___(用元素符号表示);
(3)向盛有硫酸铜水溶液的试管里加入过量氨水,得到蓝色溶液,铜离子形成了配位数为4的配离子,写出该配离子的结构式为______。
(4)由C、H、O、S中任两种元素构成甲、乙、丙三种分子,所含原子的数目依次为3、4、8,都含有18个电子。甲和乙的主要物理性质比较如下:
熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
甲 | 187 | 202 | 2.6 |
乙 | 272 | 423 | 以任意比互溶 |
①甲分子的电子式为_________,分子构型为___________;
②1 mol乙分子含有___个σ键;
③丙分子的中心原子采取_______杂化轨道;
④甲和乙的相对分子质量基本相同,造成上述物理性质差异的主要原因是 ____________(结合具体物质解释)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列各氧化还原反应中,水既不作氧化剂,也不作还原剂的是( )。
A. 2F2+2H2O==4HF+O2 B. C+H2O![]() CO+H2
CO+H2
C. 2Na+2H2O==2NaOH+H2↑ D. Cl2+H2O==HCl+HClO
查看答案和解析>>
科目: 来源: 题型:
【题目】用系统命名法命名或写出结构简式:
(1)3-甲基-2-丙基-1-戊烯的结构简式为______________________________
(2)![]() 名称为_______________________________________
名称为_______________________________________
(3)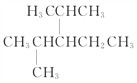 名称为:________________________________
名称为:________________________________
(4)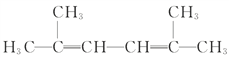 名称为:_______________
名称为:_______________
(5)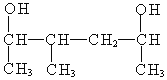 名称为:___________________________
名称为:___________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com