
科目: 来源: 题型:
【题目】2017年科学工作若研究的两项最新成果如下:
I.4-一二甲氨基吡啶( )能高效催化醋酸酐和磺胺的反应。
)能高效催化醋酸酐和磺胺的反应。
II.钙钛矿制作的一种新材料推进了人工光合作用的进程。
请回答以下问题:
(1)基态钛原子的价电子排布式为_____________________。
(2)①构成4—二甲氨基吡啶分子的各原子电负性由大到小的顺序为_____________,其中元素第一电离能最大的是_________________。
②1mol4—二甲氨基吡啶分子中所含σ键的数目为_____________,其中C原子的杂化形式为____________。(3)乙酰氯(CH3COCl)和乙酸钠(CH3COONa)反应可以制备醋酸酐。这两种反应物中熔点更高的是_____,原因是_______________________________。
(4)自然界中除钙钛矿外,碳酸钙、硫酸钙也都是钙元素形成的常见物质。请比较键角的大小:CO32-_____SO42-(填“>”“<”或“=”),推断依据是_________________________________。
(5)钙钛矿有多种晶胞结构,其中一种晶胞结构如图所示
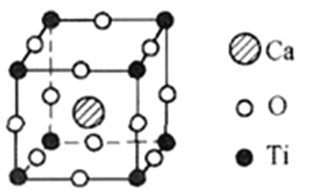
①此钙钛矿晶胞中,Ca2+周围距离最近且相等的Ca2+个数为__________________________。
②已知该晶胞的密度为d g/cm3,NA表示阿伏加德罗常数的值。计算晶胞参数a=_______pm。(写出表达式,不需要进行计算)
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的化合物应用广泛,但氮氧化物也是主要的空气污染物之一,要对其进行处理和再利用。
I.脱硝法:
(1)已知H2的燃烧热△H= -285.8kJ/mol,N2(g) +O2(g)=2NO(g) △H= + 180kJ/mol。一定条件下,H2还原NO生成液态水和一种无毒物质的热化学方程式为_______________________。
II.化合法:
工业上用NO和Cl2化合制备重要的合成用试剂NOCl( 亚硝酰氯)气体。
(2)NOCl中N 元素的化合价为__________,NOCl的电子式为_____________________。
(3)向1L恒容密团容器中通入2molNO(g)和1molCl2(g)发生反应:2NO(g) + Cl2(g)![]() 2NOCl(g) △H,在不同温度下测得c(NOCl)与时间t的关系如图所示。
2NOCl(g) △H,在不同温度下测得c(NOCl)与时间t的关系如图所示。

①该反应的△H_____0(填“>"或“<”或“=”),理由是_____________________。
②温度T1时,Cl2(g)在0~20min的平均反应速率为__________mol/(L·min)。
③温度T2时,该反应的平衡常数K=______(结果保留小数点后2位)。若反应在T2达到平衡后,再向容器中充入2molNO(g)和1molCl2(g),当再达平衡时,c(NOCl)=______(填“>”或“<”或“一”)1mol/L。
III.电化学法:
用下图所示装置可以模拟消除NO2获得铵态氮肥的过程。

(4)该装置阳极电极反应式为____________________________。
(5)电解后,向所得溶液中通入适量NH3可增加铵态氮肥的产量,理由是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据元素周期律和元素周期表,下列推断不合理的是( )
A.第35号元素的单质在常温常压下是液体
B.第四周期第ⅤA族的元素为非金属元素
C.第二周期第ⅥA族的元素的最高化合价是+6
D.第七周期0族元素的原子序数为118
查看答案和解析>>
科目: 来源: 题型:
【题目】下列措施对增大反应速率明显有效的是( )
A.在H2O2分解中加入MnO2
B.Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸
C.在NaOH与HCL两溶液反应时,增大压强
D.Na与水反应时增大水的用量
查看答案和解析>>
科目: 来源: 题型:
【题目】对同一周期主族元素从左到右递变的一般规律,叙述正确的是( )
A.最外层电子数逐渐增多
B.原子半径逐渐增大
C.最高正化合价逐渐减小
D.元素的金属性逐渐增强
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯硝酸锶[Sr(NO3)2]可用于制作红色烟火、光学玻璃、电子管阴极材料等。由工业级硝酸锶(含有硝酸钡、硝酸钙等杂质)提取高纯硝酸锶的流程如下:

(1)滤液1中的主要溶质是___________(填化学式)。
(2)相对于水洗,滤渣1用浓硝酸洗涤的优点是________________________________。
(3)滤液2中过量的铬酸洗液被N2H4还原产生Cr3+和一种不污染环境的气体。该反应的离子方程式为______________________________________。
(4)滤渣3的主要成分是_____(填化学式);滤液3中c(Cr3+)=_____mol/L(常温下Ksp[Cr(OH)3]=6.3×10-31)。
(5)操作X为_____________;Sr(NO3)2·nH2O转化为高纯硝酸锶的过程温度要控制在100℃,目的是_________________。
(6)为测定Sr(NO3)2·nH2O的数值n,将7.44g Sr(NO3)2·nH2O晶体在100℃加热至恒重为6.36g的高纯硝酸锶。计算得n=______(M[Sr(NO3)2]=212g/mol)。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲胺(CH3NH2)是一种应用广泛的一元弱碱。常温下,向200mL0.10mol/L的甲胺溶液中滴加V mL.0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是

A. b点对应加入盐酸的体积V< 20.00mL
B. 甲胺在水中的电离方程式为:CH3NH2+H2O![]() CH3NH3++OH-
CH3NH3++OH-
C. 常温下,甲胺的电离常数为Kb,则pKb=-1gKb=4.3
D. c点可能存在关系: 2c(H+)+ c(CH3NH3+)=c(CH3NH2) +2c(OH- )+ c(Cl-)
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素M、X、Y、Z、W的原子序数依次增大,X和Z同主族,M和Z原子的最外层电子数均为各自所在周期数的2倍,Y的单质燃烧火焰呈黄色。下列推断正确的是
A. 简单离子的半径:Y<Z<W
B. 最简单氢化物的沸点:X<Z<W
C. 最高价氧化物对应水化物溶液的pH:W<Z<M
D. 化合物Y2M2中既有离子键也有共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在三个体积均为 1.0L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g) + H2O(g) 下列说法正确的是( )
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
II | 387 | 0.40 | ||
III | 207 | 0.20 | 0.090 | 0.090 |
A. 该反应的正反应为吸热反应
B. 达到平衡时,容器I中的CH3OH体积分数比容器II中的小
C. 容器I中反应到达平衡所需时间比容器III的长
D. 若起始时向容器I中充入0.15mol 的CH3OH、0.15mol 的CH3OCH3和0.10mol 的H2O,则反应将向正反应方向进行
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列有关电解质溶液的叙述正确的是 ( )
A. 等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7
B. pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性
C. pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg 2=0.3)
D. 将10 mL pH=a的盐酸与100 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com