
科目: 来源: 题型:
【题目】下列关于石油的说法正确的是( )
A. 石油是混合物,汽油是纯净物
B. 石油的分馏产物是纯净物
C. 石油的裂化和裂解均为物理变化
D. 乙烯和苯是来自石油和煤的两种有机物,它们都能使溴水褪色,但褪色的原理不相同
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题:
(1)已知:
1 mol分子中的化学键断时需要吸收能量/kJ | H2(g) | Cl2(g) | HCl(g) |
436 | 243 | 431 |
则:H2(g) + Cl2(g) ![]() 2HCl(g) ΔH=____________________kJ/mol
2HCl(g) ΔH=____________________kJ/mol
(2)已知:乙醇C2H6O的燃烧热为1411.0 kJ/mol,则乙醇燃烧的热化学方程式可表示为_____________________________________________
(3)在200℃、101kPa时,H2与碘蒸气作用生成2molHI气体,放出14.9 kJ的热量。热化学方程式可表示为___________________________________________________________________。
(4)已知:① 2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(g) ΔH1=-1275.6 kJ/mol
2CO2(g)+4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO(g)+O2(g)![]() 2CO2(g) ΔH2=-566.0 k J/mol
2CO2(g) ΔH2=-566.0 k J/mol
③ H2O(g)![]() H2O(l) ΔH3=-44.0 kJ/mol
H2O(l) ΔH3=-44.0 kJ/mol
甲醇CH3OH燃烧生成一氧化碳和液态水的热化学方程式是__________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)一个SO42- 中有质子数是_____;电子数是____;含有9.6克SO42- 的(NH4)2SO4固体中,含____个氢原子,____mol NH4+。
(2)3mol CH4含有_________个分子,______mol 氢原子,此CH4的质量是____克。
(3)6 mol NH4HCO3固体的质量是____克,其中含氢原子____mol,含氧原子_____个,含阴离子和阳离子共__________个。
(4)含有6 mol K+的K2CO3的物质的量是_____,K2CO3的质量是___,阴阳离子总个数是____,氧原子的物质的量是_____。
(5)含7NA个氧原子的SO2中,SO2的物质的量是________,SO2的质量是____,氧元素的质量是_______。
(6)H2和CO的质量比为1:7时,其物质的量之比为_________,同温同压下体积之比为_____。
(7)标准状况下2.24升SO2中,m(O)=__g,含氢为4克的CH4在标况下的体积是__升。
(8)标况下3.36升NH3中含氢元素的质量是___克,含电子的个数是______。
(9)已知m(CO2)=44g,CH4的分子数为1.806×1024个。则标况下V(CO2):V(CH4)=_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的离子方程式。
(1)向Na2S2O3溶液中加入稀硫酸_____________________________________________________________
(2)在Mg(OH)2悬浊液中加入FeCl3溶液,沉淀变为红褐色____________________________________
(3)Mg(OH)2沉淀溶于NH4Cl溶液中______________________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
选项 | A | B | C | D |
物质 | MgCl2 | CO2 | HCl | NaOH |
所含化学键类型 | 离子键、共价键 | 共价键 | 离子键 | 离子键、共价键 |
所属化合物类型 | 离子化合物 | 共价化合物 | 离子化合物 | 共价化合物 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法不正确的是
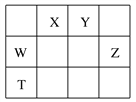
A. X、Y能形成不止一种氢化物,而Z只能形成一种
B. W和Z形成的共价化合物中,所有原子最外层均满足8电子稳定结构
C. W和T都具有良好的半导体性能
D. X和Y最多可以形成5种化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.8 mol I2(g)和1.2 mol H2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) ![]() 2HI(g) ΔH <0并达到平衡。HI的体积分数随时间的变化如表格所示:
2HI(g) ΔH <0并达到平衡。HI的体积分数随时间的变化如表格所示:
HI体积分数 | 1min | 2min | 3min | 4min | 5min | 6min | 7min |
条件I | 26% | 42% | 52% | 57% | 60% | 60% | 60% |
条件II | 20% | 33% | 43% | 52% | 57% | 65% | 65% |
下列说法中正确的是
A. 在条件I下,该反应的平衡常数K=10
B. 在条件I下,从开始反应至5min,用H2表示的反应速率为0.10 mol/(L·min)
C. 在条件II下,到达平衡时, I2(g)的转化率为81.25%
D. 与条件I相比,为达到条件II的数据,可能改变的条件是降低压强
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各物质中所含氢原子个数与3.2g O2 所含的分子数相同的是( )
A. 0.2gNH3 B. 0.1mol HCl分子
C. 6.02×1023个H2SO4分子 D. 标准状况下1.12L CH4
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度,将 0.4 mol A(g)和 0.2 mol B (g)充入 1 L 的恒容密闭容器发生反应:2A(g)+B(g)![]() xC(g)(x是化学计量数),达平衡时测得 C(g) 的浓度为 0.060mol/L,B(g)的物质的量为0.14 mol。下列说法中正确的是
xC(g)(x是化学计量数),达平衡时测得 C(g) 的浓度为 0.060mol/L,B(g)的物质的量为0.14 mol。下列说法中正确的是
A. x=2
B. 达平衡时A的转化率为40%
C. 该温度下该反应的化学反应平衡常数K=1
D. 反应前容器内的压强与平衡后容器内的压强之比为5:4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com