
科目: 来源: 题型:
【题目】NA表示阿伏加德罗常数的数值,下列有关叙述正确的是( )
①1mol苯中含有的碳碳双键数为3NA
②6.2g氧化钠和7.8g过氧化钠的混合物中含有的离子总数为0.6NA
③3.4gNH3中含N﹣H键数目为0.2NA
④常温下1L 0.5mol/L NH4Cl溶液与2L 0.25mol/L NH4Cl溶液所含NH4+的数目相同
⑤常温下4.6gNO2和N2O4混合气体中所含原子总数为0.3NA
⑥等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1
⑦1mol铁粉在1mol氯气中充分燃烧,失去的电子数为3NA
⑧高温下,16.8g Fe与足量水蒸气完全反应失去0.8NA个电子.
A. ①④⑤⑦ B. ②⑤⑧ C. ②④⑤⑦⑧ D. ⑤⑥⑦⑧
查看答案和解析>>
科目: 来源: 题型:
【题目】卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+. 表是生成氢氧化物沉淀的pH:
物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 8.1 | 3.8 | 9.5 |
完全沉淀pH | 3.7 | 9.6 | 4.8 | 11.0 |
(1)把MgCl2粗产品的溶液中的Fe2+转化为Fe3+,最适宜选用的物质是____(填序号,下同),加入______调节溶液的pH,充分反应后过滤,可得MgCl2溶液.
a.KMnO4 b.H2O2 c.MgO d.NaOH
(2)若除去溶液中的杂质离子,调节溶液的pH范围为:___________。
(3)由MgCl2溶液获得MgCl2固体的操作是:__________________。
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的Na2SO3溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-6mol·L-1],此时溶液中c(SO32-)≤__________mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则
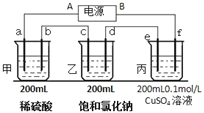
(1)电源A极是____极.
(2)2分钟后,若将乙池恢复到电解前的状态,则应加入______,加入的物质的量为______mol。
(3)丙池中发生反应的离子方程式为:________________
(4)丙装置上某极可析出固体___克,溶液的n(H+)为_____.
(5)电解n分钟后,硫酸铜正好消耗完,再将e、f电极反接电源,用同样的电流再电解n分钟,则丙溶液中的硫酸铜的物质的量浓度为______mol/L.(不考虑溶液体积变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质中既能与稀H2SO4反应,又能与NaOH溶液反应的是①Al2O3②NaHSO4③NaHCO3④Al(OH)3⑤Na2CO3( )
A.①③④B.②③⑤C.②④⑤D.①②④
查看答案和解析>>
科目: 来源: 题型:
【题目】某废水中含有的NH4+在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H =-273kL/mol
②NO2-(aq)+l/2O2(g)=NO3-(aq) △H =-73kL/mol
下列叙述不正确的是
A. lmol的NH3和1mol的NH4+都有10×6.02×1023个电子
B. 室温下,0.1mol/LHNO2(aq) pH>l,则NaNO2溶液显碱性
C. NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) △H =-346kL/mol
D. 在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
查看答案和解析>>
科目: 来源: 题型:
【题目】向氧化铁、氧化铜、铁、铜的混和粉末中加入过量的稀盐酸,充分反应后,仍有红色粉末存在,则关于溶液中阳离子的判断正确的是( )
A.只有Fe2+和Cu2+B.一定有Fe2+、Cu2+,可能有Fe3+
C.一定有Fe2+,可能有Cu2+D.只有Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用如图装置模拟该法:
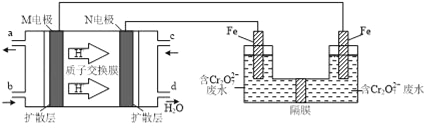
(1)N电极的电极反应式为______________________.
(2)请完成电解池中Cr2O72转化为Cr3+的离子反应方程式:______________
Cr2O72+ Fe2++ ═ Cr3++ Fe3++
(3)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×105molL﹣1 时,Cr3+沉淀完全,此时溶液的pH=_______. (已知,Ksp=6.4×1031,lg2=0.3)
(4)若燃料电池改用KOH溶液作电解质溶液,则M极的电极反应式为:____________________
(5)已知H2B在溶液中的电离方程式:H2B=H++HB﹣,HB﹣H++B2﹣.下列叙述一定正确的是(____)
A.Na2B溶液存在H2B B.NaHB溶液一定显碱性
C.NaHB溶液一定显酸性 D.NaHB溶液与稀盐酸反应的离子方程式是HB﹣+H+=H2B
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com