
科目: 来源: 题型:
【题目】下列各组物质分类正确的是( )
酸 | 碱 | 盐 | 氧化物 | |
A | 硫酸 | 纯碱 | 硫酸钙 | 氧化铁 |
B | 盐酸 | 烧碱 | 纯碱 | 氧化钙 |
C | 碳酸 | 硫酸钙 | 碳酸钠 | 干冰 |
D | 干冰 | 苛性钠 | 食盐 | 石灰石 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A. 标准状况下,2.24 L H2O所含的原子数为0.5NA
B. 1 mL 1 mol/L NaCl溶液中离子总数为2NA
C. 18 g的H2O中含有的电子数为3NA
D. 标准状况下,22.4 L氩气所含质子数为18NA
查看答案和解析>>
科目: 来源: 题型:
【题目】欧洲航天局的惠更斯号探测器首次成功登陆土星的最大卫星──土卫六。科学家对探测器发回的数据进了分析,发现土卫六的大气层中含有95%的氮气,剩余的气体为甲烷和其他碳氢化合物。下列关于碳氢化合物的叙述正确的是 ( )
A. 碳氢化合物的通式为CnH2n+2 B. 石油的主要成分是碳氢化合物
C. 乙炔是含碳量最高的碳氢氧化物 D. 碳氢氧化物中的化学键都是极性键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A.在无色溶液中:NH4+、Fe2+、SO42﹣、CO32﹣
B.在含有大量Ba2+ 的溶液中:NH4+、Na+、Cl﹣、CO32﹣
C.在强碱性溶液中:Na+、Cl﹣、K+、SO42﹣
D.在强酸性溶液中:K+、Fe2+、Cl﹣、HCO3﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】请按要求回答下列问题:
(1)请用离子方程式表示纯碱溶液呈碱性的原因:_____________________________。
(2)请用离子方程式表示明矾净水的原理:_____________________________。
(3)请用化学方程式表示氯碱工业的反应原理:_____________________________。
(4)请用化学方程式表示铝热法炼铁的反应原理:_____________________________。
(5)将AlCl3溶液蒸干并灼烧,最后得到的主要固体产物是_______________。
(6)在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+ )=c(Cl-),则溶液显_________(填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W、Q为原子序数依次增大的前四周期元素,X核外未成对电子数有2个,与其他元素均能形成二元化合物;Y是地壳中含量最多的金属元素;Z是遗传物质的组成元素之一;W内层电子数是最外层电子数的9倍;Q基态原子价层电子排布中成对电子数和未成对电子数相同。据此回答下列问题:
(1)Q的基态原子的价层电子排布式为____________________。
(2)电负性最大的是_________________,第一电离能介于Y和Z之间的同周期元素有__________ (填元素符号)。
(3)Y和W的氯化物熔点高的是_________(填化学式),原因是____________________________;与Z的低价氯化物互为等电子体的离子是_____________。
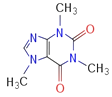
(4)咖啡因对中枢神经有兴奋作用,其结构简式如图。常温下,咖啡因在水中的溶解度为2g,加适量水杨酸钠[C6H4(OH)(COONa)]可使其溶解度增大,其原因可能是_____________________,分子中氮原子的杂化类型有_______________。
(5)已知WX的密度为3.25g/cm3,单元晶胞边长481pm,试
确定该单元晶胞中含有______个WX,属于__________立方结构(填写面心、简单或体心),晶胞中距离W最近的X有________个。
查看答案和解析>>
科目: 来源: 题型:
【题目】钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,钨在自然界主要以钨(VI) 酸盐的形式存在。有开采价值的钨矿石之一白钨矿的主要成分是CaWO4 ,含有二氧化硅、氧化铁等杂质,工业冶炼钨流程如下:

已知:
① 钨酸酸性很弱,难溶于水
② 完全沉淀离子的pH值:SiO32--为8,WO42--为5
③碳和金属钨在高温下会反应生成碳化钨
(1)74W在周期表的位置是第________周期。
(2)CaWO4与纯碱发生的化学反应方程式是_________________。
(3)滤渣B的主要成分是(写化学式)_____________。
调节pH可选用的试剂是:__________(填写字母序号)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.碳酸钠溶液
(4)母液中加入盐酸的离子方程式为____________________。
检验沉淀C是否洗涤干净的操作是:_______________________
(5)为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而须用氢气作还原剂的原因是:______________________________
将氢氧化钙加入钨酸钠碱性溶液中可得到钨酸钙,已知温度为T时Ksp(CaWO4) =1×10-10,Ksp[Ca(OH)2]= 4×10-7,当溶液中WO42-恰好沉淀完全(离子浓度等于10-5mol/L)时,溶液中![]() 等于_________________
等于_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列数量的各物质所含原子个数由大到小顺序排列的是 ( )
①0.5 mol氨气 ②4 g氦气 ③4 ℃时9 mL水 ④0.2 molH3PO4
A. ④③②① B. ①④③② C. ②③④① D. ①④②③
查看答案和解析>>
科目: 来源: 题型:
【题目】人造空气(氧气与氦气的混合气)可用于减轻某些病痛或供深水潜水员使用。标准状况下,5.6 L“人造空气”的质量是2.4 g,其中氧气与氦气的质量比是( )
A. 1∶1 B. 2∶1 C. 1∶4 D. 2∶3
查看答案和解析>>
科目: 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)已知拆开1 mol H2、1 mol O2和液态水中1 mol O—H键使之成为气态原子所需的能量分别为436 kJ、496 kJ和462 kJ;CH3OH(g)的燃烧热为627 kJ·mol-1。则CO2(g)+3H2(g)=CH3OH(g)+H2O(l) H=___________kJ·mol-1
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+ 6H2(g) ![]() CH3OCH3(g)+3H2O(l)
CH3OCH3(g)+3H2O(l)
① 该反应平衡常数表达式K=_______________。
② 已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示,该反应的H________0 (填“>”或“<”)。
若温度不变,减小反应投料比[n(H2)/n(CO2)],则K将_____(填“增大”、“减小”或“不变”)。

③某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生上述反应,当下列物理量不再发生变化时,能证明上述可逆反应达到平衡的量是__________。
A.二氧化碳的浓度 B.容器中的压强
C.气体的密度 D.CH3OCH3与H2O的物质的量之比
(3)以甲醚、空气、氢氧化钾溶液为原料的燃料电池为电源,以石墨为电极电解500mL滴有酚酞的NaCl溶液,装置如图所示:

请写出电解过程中Y电极附近观察到的现象:______________,当燃料电池消耗2.8L O2(标准状况下)时,计算此时NaCl溶液的pH=________(假设溶液的体积不变,气体全部从溶液中逸出)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com