
科目: 来源: 题型:
【题目】石油产品中除含有H2S外,还含有各种形态的有机硫,如COS、CH3SH。回答下列问题:
(1)CH3SH(甲硫醇)的电子式为________。
(2)一种脱硫工艺为:真空K2CO3—克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3,该反应的平衡常数的对数值为lgK=_____(已知:H2CO3 lgK1=-6.4,lgK2=-10.3;H2SlgK1=-7,lgK2=-19)。
②已知下列热化学方程式:
a.2H2S(g)+3O2(g)=2SO2(g)+ 2H2O(l) △H1=-1172kJ/mol
b.2H2S(g)+O2(g)=2S(s)+2H2O(l) △H2=-632kJ/mol
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为__________。
(3)Dalleska等人研究发现在强酸溶液中可用H2O2氧化COS。该脱除反应的化学方程式为______________。
(4)COS水解反应为COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H=-35.5kJ/mol。
CO2(g)+H2S(g) △H=-35.5kJ/mol。
用活性α-Al2O3催化,在其它条件相同时,改变反应温度,测得COS水解转化率如图1所示;某温度时,在恒容密闭容器中投入0.3molH2O(g)和0.1molCOS,COS的平衡转化率如图2所示。

①图1活性α-Al2O3催化水解,随温度升高转化率先增大后又减小的可能原因是________。
②由图2可知,P点时平衡常数为K=______(填数字)。
③活性α-Al2O3催化水解,为提高COS的转化率可采取的措施是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列解释事实的方程式,书写不正确的是
A. 铁与水蒸汽反应:3Fe+4H2O(g) ![]() Fe3O4+4H2
Fe3O4+4H2
B. 铝与足量NaOH溶液反应:2Al + 2OH-+ 2H2O ![]() 2AlO2-+ 3H2↑
2AlO2-+ 3H2↑
C. 稀硫酸与氢氧化钡溶液混合产生沉淀:Ba2+ + SO42- ![]() BaSO4↓
BaSO4↓
D. 用Cl2制漂白液:Cl2+2OH-=Cl-+ClO-+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】一种利用电解锰阳极泥(主要成分MnO2、MnO)制备MnO2的工艺流程如下:

(1)“煅烧氧化”时,1mol MnO煅烧完全转化为Na2MnO4失去电子的物质的量为___________;MnO2煅烧反应的化学方程式为__________________。
(2)“浸取”时,为提高Na2MnO4的浸取率,可采取的措施有____________、____________(列举2点)
(3)“调pH”是将溶液pH 调至约为10,防止pH较低时Na2MnO4自身发生氧化还原反应,生成MnO2和___________;写出用pH试纸测定溶液pH的操作_______________。
(4)“还原”时有无机含氧酸盐生成,发生反应的化学方程式为_____________。
(5)测定产品中MnO2质量分数的步骤如下:
步骤1. 准确称取mg产品,加入c1mol·L-1Na2C2O4溶液V1mL (过量)及适量的稀硫酸,水浴加热煮沸一段时间。(已知:Na2C2O4+2H2SO4+MnO2=MnSO4+2CO2↑+2H2O+Na2SO4)
步骤2. 然后用c2mol·L-1KMnO4标准溶液滴定剩余的Na2C2O4滴定至终点时消耗KMnO4标准溶液V2mL。(已知:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O)
步骤2达滴定终点时判断依据是_____________;产品中MnO2的质量分数为ω(MnO2)=____________(列出计算的表达式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某校同学在实验室中对一氧化碳与硫酸钙反应进行了探究。回答下列问题:
(1)甲组同学利用CaSO4·2H2O在400--500℃脱水制取无水CaSO4。实验中需用到的加热装置中的硅酸盐质的仪器除玻璃棒外,还用到______________。
(2)乙组同学利用H2C2O4·2H2O在浓硫酸作用下脱水生成CO、CO2并制备纯净的CO气体,实验装置如下:

B、C中盛放的试剂依次为______、____________。
(3)丙组同学利用甲组制得的无水CaSO4和乙组制得的CO并利用下列装置验证反应并检验气态产物中有SO2和CO2产生。

①上述装置(部分装置可重复使用)的连接顺序为C→___________。
②若E溶液褪色,则发生反应的离子方程式为_____________。
③能证明有CO2的生成的实验依据是____________。
④若G中产物为CaO,则G中发生反应的化学方程式为_________________。
(4)丁组的同学取丙组实验后G装置中的固体产物加入试管中,然后加人足量稀盐酸,固体完全溶液且产生少量气体,通入CuSO4溶液有黑色沉淀。可验证CO与CaSO4在高温下还发生了一个副反应,该反应为______________(用方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)
后使用。请回答下列问题:
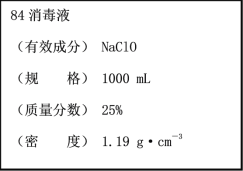
(1)该“84消毒液”的物质的量浓度约为_____mol·L-1。
(2)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是________(填字母)。
A.溶液中NaClO的物质的量 B.溶液的浓度
C.溶液中NaClO的摩尔质量 D.溶液的密度
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。回答下列问题。
①如图所示的仪器中,有些是不需要,配制上述溶液还需要_____________玻璃仪器
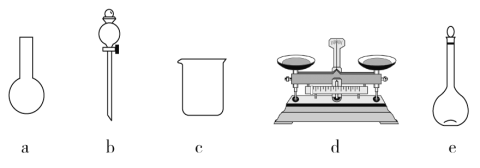
②需要称量NaClO固体的质量为_______ g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制200 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________ mol·L-1。
②需用浓硫酸的体积为________ mL。
③若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是_______。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,仰视溶液的凹液面
查看答案和解析>>
科目: 来源: 题型:
【题目】有关 98%的浓硫酸的问题叙述错误的是:
A. 硫酸和水的物质的量比9:1
B. 物质的量浓度大于10 mol·L-1
C. 和水等体积混合,所得溶液质量分数大于49%
D. 和水等质量混合,所得溶液质量分数大于49%
查看答案和解析>>
科目: 来源: 题型:
【题目】由下列实验及现象得出的结论正确的是
实验 | 现象 | 结论 | |
A | SO2与H2S气体混合 | 产生淡黄色沉淀 | 氧化性:SO2>S |
B | 向盛有FeSO4溶液的试管中滴入氯水,然后滴入KSCN溶液 | 滴入KSCN后溶液变为红色 | 原FeSO4溶液已被空气中O2氧化变质 |
C | 试管中盛有Cu(NO3)2溶液,底部有少量铜,向其中加入稀硫酸 | 铜粉逐渐溶解 | 铜可与稀硫酸反应 |
D | 向2支盛有2mL相同浓度的NaOH溶液的试管中分别滴入2滴相同浓度的AlCl3和MgCl2溶液,振荡并静置 | 前者无沉淀,后者有白色沉淀 | Ksp[Al(OH)3]>Ksp[Mg(OH)2] |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的变化,不能通过一步化学反应完成的是( )
A.Na2O2→Na2CO3B.Fe→FeCl2C.SiO2→H2SiO3D.Na2CO3→NaHCO3
查看答案和解析>>
科目: 来源: 题型:
【题目】《天工开物》中记载了古人冶金、制陶瓷、硫磺、火药等的过程,是我国古代闪耀的“科技之光”,下列冶炼铁的过程中发生化学变化的是
A.凡铁场所在有之,其铁浅浮土面,浮者拾之 | B.取来淘洗 | C.入炉熔化 | D.凡铁一炉载土二千余斤,或用硬木柴,或用煤炭,或用木炭,土化成铁 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com