
科目: 来源: 题型:
【题目】下列说法中,不正确的是( )
A.全部由非金属元素形成的化合物一定是共价化合物
B.离子化合物中可能含有非极性键
C.共价化合物中肯定不含有离子键
D.化学变化过程,一定会破坏旧的化学键,同时形成新的化学键
查看答案和解析>>
科目: 来源: 题型:
【题目】(题文)有关下列有机物的说法中错误的是
A. 石油经分馏后再通过裂化和裂解得到汽油
B. 植物油通过氢化加成可以变成脂肪
C. 用灼烧的方法可以区别蚕丝和合成纤维
D. 在做淀粉的水解实验时,用碘水检验淀粉是否完全水解
查看答案和解析>>
科目: 来源: 题型:
【题目】单晶硅是信息产业中重要的基础材料.通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝,硼,磷等杂质).粗硅与氯气反应生成四氯化硅(反应温度450—500 ℃),四氯化硅经提纯后用氢气还原可得高纯硅。
氯气的制取:

(1)实验室用MnO2和浓盐酸制取氯气,若要制得干燥,纯净的氯气,所需装置的接口连接顺序是 ___(填小写字母)。
(2)写出实验室制取氯气的离子方程式:____ 。
(3)装置A中恒压分液漏斗M与常用分液漏斗相比,其优点是 _____,装置D的作用是____。
将上述方法制取的氯气通入下图装置中可以制得四氯化硅。
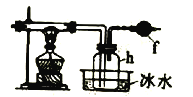
[资料]
a.四氯化硅遇水极易水解
b.硼、铝、铁,磷在高温下均能与氯气直接反应生成相应的氯化物
c.有关物质的熔沸点见下表:
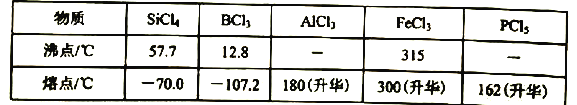
(4)装置f中盛放的药品是____,h瓶中左边用粗导管导出物质的目的是____。
(5)从b瓶得到的液体中蒸馏出SiCl4,所需用到的仪器是 ___。
A.容量瓶 B.温度计 C.冷凝管 D.分液漏斗
(6)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O 。某同学称取5.000 g残留物,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000 × 10-2 mol·L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00mL,滴定终点的现象是____,残留物中铁元素的质量分数是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是()
A. 能电离出离子的化合物都是离子化合物
B. 熔融状态下能导电的化合物一定是离子化合物
C. 不同元素组成的多原子分子里的化学键一定是极性键
D. 非金属元素构成的单质中一定存在共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是:
A. 化学能可以转变成为热能、电能等
B. 化学反应中的能量变化主要是由化学键的变化引起的
C. 化学反应必然伴随发生能量变化
D. 化学反应中能量变化的多少与反应物的质量无关
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:一定条件下,向A、B两个恒容密闭容器中分别加入等量的X(容器内所有物质均为气体),测得A、B容器中X的物质的量n(X)随时间t的变化如图所示。下列说法正确的是
A. A.B容积相同,但反应温度不同.且温度:A>B
B. A、B反应温度相同,但容积不同,且容积:A>B
C. a,b,c三点对应的平均相对分子质量:b>c>a
D. t2-t3时间段内,A、B两容器中平均反应速率相等
查看答案和解析>>
科目: 来源: 题型:
【题目】下列措施不能加快Zn与1mol/LH2SO4反应产生H2的速率的是
A. 升高温度 B. 用Zn粉代替Zn粒
C. 改用发烟H2SO4与Zn反应 D. 滴加少量的CuSO4溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】有人设想以N2和H2为反应物,以溶有X的稀盐酸为电解质溶液,制造出新型燃料电池,装置如图所示。下列说法正确的是
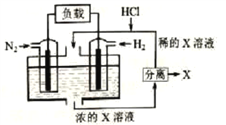
A. 放电时H+向左移动,生成的物质X是NH4Cl
B. 通入H2的一极为正极
C. 通入N2的电极反应为:N2+6H+-6e-=2NH3
D. 放电过程右边区域溶液pH逐渐增大
查看答案和解析>>
科目: 来源: 题型:
【题目】有关键能数据如表
化学键 | Si—O | O=O | Si—Si |
键能/kJ·mol-1 | x | 498.8 | 176 |
晶体硅在氧气中燃烧的热化学方程式:Si(s)+O2(g)=SiO2(s);ΔH=-989.2 kJ·mol-1,则表中x的值为 ( )
A.460B.920
C.1165.2D.423.3
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需0.5mol/L的Na2CO3溶液970mL和0.5mol/L硫酸溶液250mL.根据这两种溶液的配制情况回答下列问题:
(1)下列仪器使用前必须检查是否漏水的有_________(填序号)。
A.容量瓶 B.蒸馏烧瓶 C.分液漏斗 D.量筒 E.蒸发皿
(2)实验室需0.5mol/L的Na2CO3溶液970mL,现用用Na2CO3·10H2O晶体配制。
①所需仪器除了烧杯、玻璃棒、量筒、托盘天平、药匙外,还缺少_____________、_______________;
根据计算用托盘天平称取Na2CO3·10H2O的质量是_______________ g。
②下图是某同学在实验室配制该溶液的过程图,其中有错误的是______________ (填操作序号)。

(3)某学生欲用质量分数为98%、密度为1.84g/cm3的浓硫酸和蒸馏水配制0.5mol/L硫酸溶液250mL。
①该学生需要用量筒量取________mL上述浓硫酸进行配制。
②配制硫酸溶液时,其正确的操作顺序是B→C → ______→______→____→D。
A.用30 mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,轻轻摇动容量瓶
B.用量筒准确量取所需浓硫酸的体积,慢慢沿杯壁注入盛有适量水的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的硫酸沿玻璃棒注入容量瓶中
D.将容量瓶的玻璃塞盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处
③在配制过程中,下列操作会使所配制的稀硫酸物质的量浓度偏低是__________(填字母序号)。
A.定容时仰视刻度线 B.溶液注入容量瓶前没有恢复到室温就进行定容
C.容量瓶使用前未经干燥 D.用量筒量取浓硫酸时俯视观察凹液面
E. 未将量取浓硫酸的量筒进行洗涤
F.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com