
科目: 来源: 题型:
【题目】I. E的产量是衡量一个国家石油化工水平发展的标志,F为高分子化合物,能进行如图所示的反应。

(1)请写出E的电子式_______________。
(2)下列反应的化学方程式:(要求有机物必须写结构简式)
反应②:________________________ 反应类型________。
反应③:________________________ 反应类型________。
反应④:____________________反应类型________。
反应⑤:____________________反应类型________。
(3)比较反应①剧烈程度_____________(填>、= 或<)钠和水反应的剧烈程度。
Ⅱ.2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭。“亮菌甲素”的结构简式为:

它配以辅料丙二醇溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性。请回答下列问题:
(1)下列有关“亮菌甲素”的叙述正确的是________(填字母)。
A.“亮菌甲素”能与H2发生加成反应 B.不能使酸性KMnO4溶液褪色
C.“亮菌甲素” 的分子式是C12H10O5 D.“亮菌甲素”分子中含氧官能团只有2种
(2)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在。写出其所有属于醇类的同分异构体的结构简式_______________________________。
(3)依据核磁共振氢谱分析,二甘醇分子中有3个吸收峰,其峰面积之比为2∶2∶1。又知二甘醇中含碳、氧元素的质量分数相同,且氢元素的质量分数为9.4%,1 mol二甘醇与足量金属钠反应生成1 mol H2。写出二甘醇的结构简式________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组学生根据氧化还原反应规律,探究NO2、NO与Na2O2反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析Na2O2和NO2都既有氧化性又有还原性,于是提出如下假设:
假设1:Na2O2氧化NO2;假设2:NO2 氧化Na2O2。
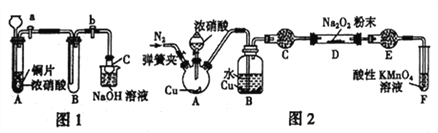
(1)甲同学设计如图1装置进行实验:
①试管A 中反应的离子方程式是____________________________。
②待试管B 中充满红棕色气体,关闭旋塞a和b;取下试管B;向其中加入适量Na2O2粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
③仪器C兼有防倒吸的作用,仪器C的名称为___________________。
结论:甲同学认为假设2 正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是________________________。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设1正确,则NO2和Na2O2反应的化学方程式是_______________________。
Ⅱ.该研究性学习小组同学还认为NO 易与O2发生反应,应该更易被Na2O2氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O; 酸性条件下,NO 能与MnO4-反应生成NO3-和Mn2+。
(3)丙同学用图2所示装置(部分夹持装置略)探究NO与Na2O2的反应。
①在反应前,打开弹簧夹,通入一段时间N2,目的是_________________。
②B 中观察到的主要现象是____________(填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色 b.有红棕色气泡产生 C.有无色气泡产生③C、E 中所盛装的试剂不能是________(填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④F 中发生反应的氧化剂与还原剂的物质的量之比为_____________。
⑤充分反应后,检验D装置中产物的方法是:______________ ,则产物是NaNO2。
查看答案和解析>>
科目: 来源: 题型:
【题目】当物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液中所含Cl-的个数相等时,这三种溶液的体积比应是( )
A. 1∶1∶1 B. 1∶2∶3 C. 3∶2∶1 D. 6∶3∶2
查看答案和解析>>
科目: 来源: 题型:
【题目】现有14.4gCO和CO2的混合气体,在标准状况下其体积为 8.96L。请回答下列问题:
(1)该混合气体的平均摩尔质量 为 _____。
(2)该混合气体 中碳原子的个数 为 _____;(用N A表示阿伏加德罗常数的值)
(3)将该混合气体依次通过如下图所示装置,最后收集在气球中(体积在标准状况下测定) .

气球中收集到的气体的摩尔质量 _____;
② 气球中收集到的气体的电子总数为 _____;(用 NA表 示阿伏加德罗常数的值 )
③ 标况下气球中收集到的气体的体 积为 _____L。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中,正确的是
A. 甲烷是一种清洁能源,是天然气的主要成分
B. 用KMnO4溶液浸泡过的藻土可使水果保鲜,是利用了乙烯的氧化性
C. 苯不能使KMnO4酸性溶液褪色,说明它是一种饱和烃,很稳定
D. 己烷可以使溴水褪色,说明己烷中含有碳碳双键
查看答案和解析>>
科目: 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接着4个不同的原子或原子团,则这种碳原子称为“手性碳原子”。凡有一个手性碳原子的物质一定具有光学活性,物质![]() 有光学活性,发生下列反应后生成的产物有光学活性的是( )
有光学活性,发生下列反应后生成的产物有光学活性的是( )
A. 与NaOH水溶液共热 B. 与银氨溶液作用
C. 与乙酸发生酯化反应 D. 在催化剂存在下与H2作用
查看答案和解析>>
科目: 来源: 题型:
【题目】主族元素在元素周期表中的位置,取决于元素原子的( )
A.相对原子质量和核电荷数B.电子层数和中子数
C.电子层数和最外层电子数D.电子层数和核外电子数
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
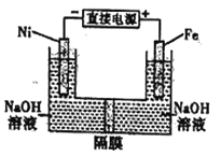
A. 若隔膜为阴离子交换膜,则OH-自右向左移动
B. 铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+8H+
C. 电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
D. 电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgc(M2+)]与溶液pH的变化关系如图所示,已知该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2]。下列说法正确的是

A. 曲线a表示Fe(OH)2饱和溶液中的变化关系
B. 除去CuSO4溶液中含有的少量Fe2+,可加入适CuO
C. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中c(Fe2+):c(Cu2+)=104.6 :1
D. 向X点对应的饱和溶液中加入少量NaOH固体,可转化为Y点对应的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com