
科目: 来源: 题型:
【题目】下表列出了前20号元素中的某些元素性质的一些数据:
元素 性质 | A | B | C | D | E | F | G | H | I | J |
原子半径 (10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
最高 价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
最低 价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)以上10种元素中,电负性最大的是________(填元素符号)。
(2)写出下列有关反应的化学方程式:
①E的单质与I元素的最高价氧化物对应的水化物浓溶液反应方程式:________________。
②B2C2与EC2反应:________________________。
(3)比元素B原子序数大10的元素的原子的电子排布式是________。
(4)C和I相比较,非金属性较弱的是_____(填元素名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是
A. 溶液中导电粒子的数目增加,导电性增强
B. 醋酸的电离程度增大,c(H+)亦增大
C. 再加入10mL pH=11 NaOH溶液,混合液pH=7
D. 溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]不变
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘化钾(即碘离子)的形式存在。实验室里从海藻中提取碘的流程如下图,已知 (Cl2+2KI=2KCl+I2)
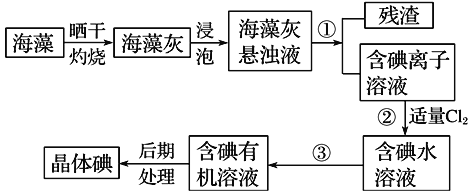
(1)实验室焙烧海带,需要下列仪器中的________(填字母)。
a.试管 b.烧杯c.坩埚 d.泥三角 e.三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①________,③__________。
(3)提取碘的过程中,可选择的有机试剂是________。
A.苯、酒精 B.四氯化碳、苯 C.汽油、醋酸 D.汽油、酒精
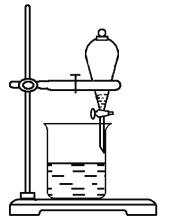
(4)某小组用CCl4萃取碘水中的碘,在如图的分液漏斗中,下层液体呈______色;他们打开分液漏斗活塞,却未见液体流下,原因可能是___________________ 。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
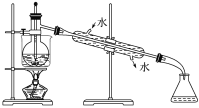
①________________________________________________;
②______________________________________________________;
③________________________________________________________。
(6)进行上述蒸馏操作时,使用水浴加热的目的_______________________,最后晶态碘在________里聚集。
查看答案和解析>>
科目: 来源: 题型:
【题目】周期表前四周期的元素X、Y、Z、T、W,原子序数依次增大。X的核外电子总数与其周期数相同,Y基态原子的p电子数比s电子数少1个,Z基态原子的价电子层中有2个未成对电子,T与Z同主族,W基态原子的M层全充满,N层只有一个电子。回答下列问题:
(1)Y、Z、T中单质熔点最高是______(填元素符号)
(2)比W原子序数少5的基态原子中单电子数为_________________。
(3)T与Z形成的化合物中,中心原子杂化类型是_______
(4)X和上述其他元素中的一种形成的化合物中:分子呈三角锥形的是________(填化学式);分子中既含有极性共价键,又含有非极性共价键的化合物是_______(填化学式,写一种)。
(5)这5种元素形成的一种阴阳离子个数比为1:1型的配合物中,阴离子呈四面体结构,阳离子的结构如图所示。该配合物的化学式为__________,阳离子中存在的化学键类型有_______。
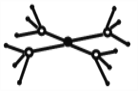
查看答案和解析>>
科目: 来源: 题型:
【题目】铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:

①Cu2+的价电子排布图________________; NH4CuSO3中N、O、S三种元素的第一电离能由大到小顺序为_______________________(填元素符号)。
②SO42-的空间构型为_____________,SO32-离子中心原子的杂化方式为__________。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式:___________。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是________
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因_____________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】熏衣草醇( 结构如图) 可以用于高级化妆品及香水的香料。下列有关熏衣草醇的说法正确的是
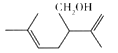
A. 熏衣草醇的分子式为C10H16O
B. 薰衣草醇能发生加成反应和酯化反应
C. 熏衣草醇分子中所有碳原子可能处于同一个平面
D. 熏衣草醇使溴水和酸性KMnO4 溶液褪色的原理相同
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列有关叙述正确的是
A. 46g乙醇与甲酸混合物中,含有的氧原子数为NA
B. 1L0.1mol/L的CH3COONa溶液中,Na+数为0.1NA
C. 标准状况下,5.6LNO和O2的混合气体中含有的分子数为0.25NA
D. 常温下,14g铁皮与足量浓硝酸反应,转移的电子数为0.75NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A. sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道
B. 乙炔分子中,每个碳原子都有两个未杂化的2p轨道形成π键
C. 凡中心原子采取sp2杂化的分子,其分子构型都是平面三角形
D. 凡AB2型的共价化合物,其中心原子A均采用sp杂化轨道成键
查看答案和解析>>
科目: 来源: 题型:
【题目】t℃时,向xgKNO3不饱和溶液中,加入agKNO3或蒸发掉bg水恢复到t℃,溶液均达到饱和,据此下列推论错误的是
A. 在t℃时,KNO3的溶解度为100a/b g
B. 若原溶液中溶质质量分数为![]() ,则x=2b
,则x=2b
C. 若原不饱和溶液蒸发掉2b g水,恢复到原温度,能析出2a gKNO3
D. 在t℃时所配得的KNO3溶液中溶质质量分数≤![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B. FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2=2Fe3++2H2O
C. 用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D. 电解MgCl2水溶液的离子方程式:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com