
科目: 来源: 题型:
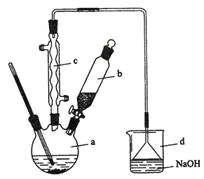
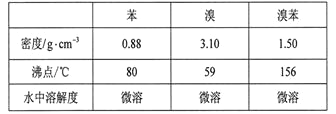
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了________气体。继续滴加至液溴滴完。装置d的作用是________________;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用l0 mL水、8 mL l0%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必须是______(填入正确选项前的字母);
A重结晶 B过滤 C蒸馏 D萃取
(4)在该实验中,a的容积最适合的是______(填入正确选项前的字母)。
A、25 mL B、50 mL C、250 mL D、509 mL
查看答案和解析>>
科目: 来源: 题型:
【题目】降低大气中C02的含量及有效地开发利用CO2,已引起了全世界的普遍重视。
(1)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一。
①2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)△H= -122.4kJ·mol-1
CH3OCH3(g)+3H2O(g)△H= -122.4kJ·mol-1
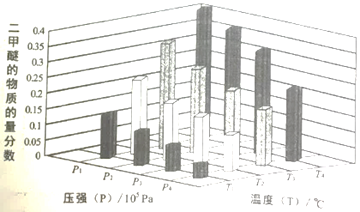
某温度下,将2.0molCO2(g)和6.0molH2(g)充入容积为2L的密闭容器中,反应到达平衡时、改变压强和温度,平衡体系中CH3OCH3(g)的物质分数变化情况如图所示,则p1______p2(填“>”“<”或“=”,下同)。若T1、P1,T3、P3时平衡常数分别为K1、K3,则K1______K3,T1、P1时H2的平衡转化率为____________。
②在恒容密闭容器里按体积比为1:3充入二氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列能说明平衡一定向逆反应方向移动的是______(填序号)。
A. 反应物的浓度增大 B. 混合气体的密度减小
C. 正反应速率小于逆反应速率 D. 氢气的转化率减小
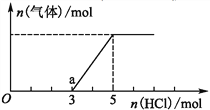
(2)将一定量的CO2气体通入氢氧化钠的溶液中,向所得溶液中边滴加稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。请回答:通入1mol HCl时,溶液中所含溶质的化学式_____________,a点溶液中各离子浓度由大到小的关系式为___________________。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其![]() 。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为
。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为![]() mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为__________mol·L-1.
mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为__________mol·L-1.
查看答案和解析>>
科目: 来源: 题型:
【题目】某种碳酸锰矿的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等。已知碳酸锰难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下:

(1)写出用稀硫酸溶解碳酸锰反应的离子方程式______________________________。
(2)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.3 |
沉淀完全的pH | 3.7 | 4.7 | 9.6 | 9.8 | 10.8 |
①流程中先加双氧水的目的是__________________________________________。
②加氨水调节溶液的pH等于6,则滤渣的成分是__________________,滤液中含有的阳离子有H+ 和___________________。
(3)在浸出液里锰元素只以Mn2+ 的形式存在,且滤渣中也无MnO2,请解释原因_________。
(4)阴离子膜法电解装置如右图所示,电解装置中箭头表示溶液中阴离子移动的方向,则A电极是______极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为__________________________。

(5)该工艺之所以采用阴离子交换膜,是为了防止Mn2+ 进入阳极区发生副反应生成MnO2造成资浪费,写出该副反应的电极反应式________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用右图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 | 实验装置 |
A | 稀硫酸 | Na2S | AgNO3与AgCl的溶液 | Ksp(AgCl)>Ksp(Ag2S) |
|
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四种X溶液,均能跟盐酸反应,其中反应最快的是( )
A.10℃20mL 3mol/L的X溶液
B.20℃30mL 2molL的X溶液
C.20℃10mL 4mol/L的X溶液
D.10℃10mL 2mol/L的X溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)有下列五种烃:

其中互为同分异构体的是_________________(填序号),②③④⑤四种物质按它们的沸点由低到高的顺序是________________(填序号),等质量的①③⑥三种物质,完全燃烧时消耗O2的物质的量由少到多的顺序为________________ 。
(2) 的系统命名为___________________;
的系统命名为___________________;
(3)分子式为C2H6O的有机物,有两种同分异构体,乙醇(CH3CH2OH)、二甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是 ______
A.红外光谱 B. 1H核磁共振谱 C.质谱法 D.与钠反应
(4)已知乙烯分子是平面结构, 1,2-二氯乙烯可形成![]() 和
和![]() 两种不同空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是_____
两种不同空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是_____
A.1-丙烯 B.4-辛烯 C.1-丁烯 D.2-甲基-1-丙烯
查看答案和解析>>
科目: 来源: 题型:
【题目】已知微粒间的相互作用有以下几种:
①离子键 ②极性共价键 ③非极性共价键 ④氢键 ⑤分子间作用力
下面是某同学对一些变化过程破坏的微粒间的相互作用的判断:
A.干冰熔化②⑤ B.氢氧化钠溶于水①
C.氯化氢气体溶于水 ②④ D.冰熔化②④
其中判断正确选项的是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为Y2X3(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是( )
A. 原子半径:Y>Z>R>T B. 气态氢化物的稳定性:W<R<T
C. 最高价氧化物对应的水化物的碱性:X>Z D. XR2、WR2两种化合物中R的化合价相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com