
科目: 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,回答有关问题:
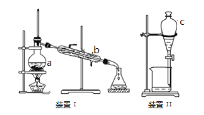
(1)写出装置I中有关仪器的名称:a ________________,b__________________,该装置分离混合物的原理是根据混合物各组分______________不同进行分离的。
(2)装置II中仪器C 的名称为_______________,使用C前必需进行的操作是 _______________为使C中液体顺利流下,打开活塞前应进行的操作是 _________________________。
(3)下面是用36.5%的浓盐酸(ρ=1.19g/cm3)配制250mL 0.5mol/L的稀盐酸 的操作,请按要求填空:
①配制上述溶液所需的玻璃仪器除玻璃棒、量筒、烧杯,还有 _____________________,需要量取浓盐酸的体积为 ____________mL。
②下列操作中,会造成所配溶液浓度偏低的是______(填字母)。
a.定容时,俯视刻度线 b.没有洗涤烧杯和玻璃棒
c.洗涤后的容量瓶中残留少量蒸馏水。d.量筒量取盐酸前没有用浓盐酸润洗。
③经测定,所配溶液的浓度偏小,如果忽略实验过程产生的误差,可能的原因是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】酶指具有生物催化功能的高分子物质.在酶的催化反应体系中,反应物分子被称为底物,底物通过酶的催化转化为其他分子.几乎所有的细胞活动进程都需要酶的参与,以提高效率.请回答下列问题:
(1)酶氧化酶与酚类底物在细胞中能实现分类存放,是因为细胞内具有 系统,组成该系统的结构具有的功能特性是 .茶叶细胞中也存在众多种类的酚类物质与酚氧化酶.绿茶制取过程中必须先进行热锅高温炒制,这一过程的目的是 .
(2)茶树的Rubicon酶在CO2浓度较高时,该酶催化C2与CO2反应,Rubicon酶的存在场所为 ;该酶具有“两面性”,在O2浓度较高时,该酶催化C2与O2反应,产物经一系列变化后到线粒体中会产生CO2,其“两面性”与酶的 (特性)相矛盾.
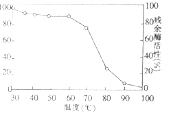
(3)如图中曲线表示将酶在不同温度下保温足够长时间,再在酶活性最高的温度下测其残余酶活性,由图可得出: .为了验证这一结论,请以耐高温的纤维素分解酶为实验材料,比较在低温和最适温度下储存对酶活性的影响,写出实验设计思路: .
查看答案和解析>>
科目: 来源: 题型:
【题目】有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥环己烯;⑦聚丙烯.其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是
A. ①③⑤ B. ④⑥⑦ C. ①④⑦ D. ②③⑤
查看答案和解析>>
科目: 来源: 题型:
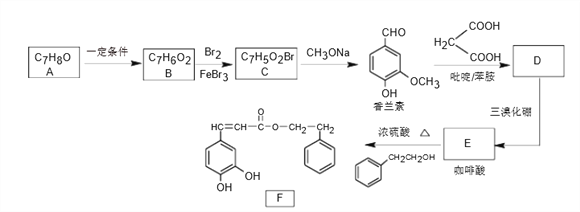
【题目】化合物F具有独特的生理药理作用,实验室由芳香化合物A制备F的一种合成路线如下:
已知:①R-Br![]() R-OCH3 ②R-CHO+
R-OCH3 ②R-CHO+![]() R-CH=CH-COOH
R-CH=CH-COOH
③A能与FeCl3溶液反应显紫色
(1)A的名称为_________________,B生成C的反应类型为__________________。
(2)D的结构简式为________________________。
(3)E中含氧官能团名称为_______________。
(4)写出F与足量NaOH溶液反应的化学方程式__________________________。
(5)G为香兰素的同分异构体,其中能同时满足下列条件的共有______种。(不考虑立体异构)
①能发生银镜反应
②本环上只有3个取代基
③1molG能与足量金属钠反应产生22.4LH2(标准状况)其中核磁共振氢谱有5组峰,且峰面积比为1∶1∶2∶2∶2的结构简式__________。(写一种即可)
(6)根据上述合成中提供的信息,写出以![]() 为原料(其他试剂任选)分三步制备肉桂酸(
为原料(其他试剂任选)分三步制备肉桂酸(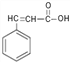 )的合成路线。_____________________________________________
)的合成路线。_____________________________________________
查看答案和解析>>
科目: 来源: 题型:
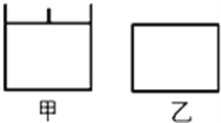
【题目】已知甲为恒压容器、乙为恒容容器.相同条件下充入等物质的量的NO2气体,且起始时体积相同,发生反应:2NO2(g)N2O4(g)△H<0.一段时间后相继达到平衡状态..下列说法中错误的是( )
A. 该反应的平衡常数表达式K=c(N2O4)/c2(NO2)
B. 若乙容器内气体的压强保持不变,说明反应已达到平衡状态
C. 平衡时NO2体积分数:甲>乙
D. 达到平衡所需时间,甲所需时间短
查看答案和解析>>
科目: 来源: 题型:
【题目】石英晶体的平面示意图如图所示,它实际上是网状结构,其中硅、氧原子的个数比是m:n,有关叙述正确的是( )(相对原子量Si 28 O 16)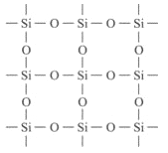
A. 6g该晶体中含有0.1NA个分子
B. m:n=2:1
C. 原硅酸根SiO44—的结构为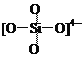 ,则二聚硅酸根离子Si2O7x—中的x=6
,则二聚硅酸根离子Si2O7x—中的x=6
D. 六聚硅酸根[Si6O18]y—中的y=10
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、C、D,原子序数依次增大,A的基态原子的L层电子是K层电子的两倍;B的价电子层中的未成对电子有3个;C与B同族;D的最高价含氧酸为酸性最强的无机含氧酸。请回答下列问题:
(1)C的基态原子的电子排布式为___________;D的最高价含氧酸酸性比其低两价的含氧酸酸性强的原因是_____________________________________________。
(2)杂化轨道分为等性和不等性杂化,不等性杂化时在杂化轨道中有不参加成键的孤电子对的存在。A、B、C都分别能与D形成中心原子杂化方式均为___________的共价化合物X、Y、Z。其中,属于不等性杂化的是___________ (写化学式)。
(3)比较Y、Z的熔沸点Y______Z(填“>”、“<”或“=”),并解释理由_____________________。
(4)D元素能与Cu形成棕黄色固体,加水溶解并稀释过程中,溶液颜色由绿色逐渐转化为蓝色,显绿色离子是_________________,显蓝色离子中的配位原子________________。
(5)A和B能形成多种结构的晶体。其中一种类似石墨的结构,其结构如下图所示(图1为晶体结构,图2为切片层状结构),其化学式为__________。实验测得此晶体结构属于六方晶系,晶胞结构见图3。已知图示原子都包含在晶胞内,晶胞参数a=0.64nm,c=0.24nm。其晶体密度为__________g/cm3(已知:2=1.414,后=1.732,结果精确到小数点后第2位。)
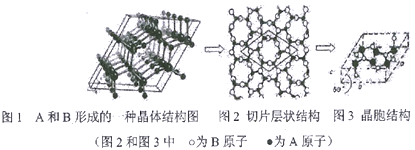
查看答案和解析>>
科目: 来源: 题型:
【题目】在Fe、Cu、稀H2SO4组成的原电池中。下列叙述错误的是
A.电子流从铁棒经导线流入铜棒B.溶液逐步变为浅绿色
C.溶液的酸性减弱D.气泡在铁片上产生
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是实验室制取少量固体氧化铜的实验,根据实验步骤,回答有关问题。

(1)调整天平零点时,若指针偏向右边,应将左边的螺丝____________(填“向左”或“向右”)旋动。
(2)滴加NaOH溶液,生成沉淀的离子方程式为_______________________________。
(3)加热蒸发过程中要用到玻璃棒,其作用是_________________________________。
(4)洗涤该沉淀的方法是______________________________________________________,为了检验此沉淀是否洗涤干净,应取最后一次的洗涤液少许,加入__________溶液检验。
(5)若向CuSO4溶液中滴加了100mLNaOH溶液,则NaOH溶液的物质的量浓度至少为_________。
(6)理论上最多可以制得CuO的质量为 _______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮氧化物排放是形成臭氧层空洞、酸雨、雾霾的重要成因之一
I.NO和CO气体均为汽车尾气的成分,目前降低尾气的可行方法是在汽车排气管上安装催化转化器,这两种气体在催化转换器中发生反应:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H
N2(g)+2CO2(g) △H
已知反应中相关键能数据如下:
化学键 | C | N | N | C=O |
键能/kJ·mol-1 | 1076 | 632 | 946 | 750 |
(1)由此计算△H=__________。
(2)在一定温度下,将2.0molNO、2.4molCO通入到容积固定为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:
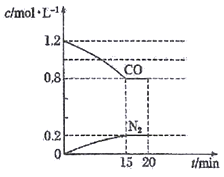
①有害气体NO的转化率为__________。
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是__________ (填序号)。
a.缩小容器体积 b.催化剂 c.降低温度 d.再通入2.0molNO
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,平衡将__________ (填“正向”或“逆向”)移动。
Ⅱ.SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为:4NO(g)+4NH3(g)+O2(g)![]() 4N2(g)+6H2O(g)△H<0
4N2(g)+6H2O(g)△H<0
(3)该法可能发生副反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),减少副反应的主要措施是___________(写一条即可)。
4NO(g)+6H2O(g),减少副反应的主要措施是___________(写一条即可)。
(4)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
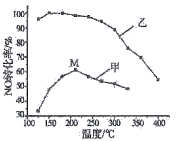
①工业上选择催化剂__________(填“甲”或“乙”),原因是____________。
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率______(填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是__________。(写一条即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com