
科目: 来源: 题型:
【题目】(1).2Na+2H2O=2NaOH+H2↑为氧化还原反应
氧化剂是_________ 还原剂是________
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮直至溶液呈____________色,即可制得Fe(OH)3胶体。
(3)Fe(OH)3胶体,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫________;胶体中加入电解质,胶体变得浑浊,这是发生了__________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A. 若丙醇中的氧为188O,它与乙酸反应生成的酯的相对分子质量是102
B. 油酸、苯丙氨酸、葡萄糖分子中均含有两种官能团
C. 由![]() 在浓硫酸加热170℃可发生消去反可制备CH3—CH═CH2
在浓硫酸加热170℃可发生消去反可制备CH3—CH═CH2
D. 用乙酰水扬酸![]() 与适量NaOH溶液反应制备
与适量NaOH溶液反应制备![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】80年代,科学研制得一种新分子,它具有空心的类似足球状的结构,分子式为C60 . 下列说法正确的是( )
A.C60是一种新型的化合物
B.C60含有离子键
C.C60和金刚石互为同位素
D.C60中的化学键只有共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】C、N、O、S、H都是中学化学中常见的元素。按要求完成下列填空。
(1)0.5 mol CH4的质量为____________;标准状况下,4.48 L NH3所含分子数为___________。
(2)等物质的量的CH4、NH3和N2三种气体,所含原子数之比为__________,等质量的CH4和N2物质的量之比为__________。
(3)含有1.806×1024个电子的OH- 的物质的量为____;0.5 mol H2O分子中所含电子数与_____个NH4+中所含电子数相等。
(4)在标准状况下,由SO2和CO2组成的混合气体为8.96 L,质量为24 g,该混合气体的平均摩尔质量是__________,混合气体中CO2的体积分数是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】镭是周期表中第7周期第ⅡA主族元素,下列关于镭的性质描述中不正确的是( )
A.在化合物中呈+2价
B.镭比钙的金属性强
C.氢氧化物呈两性
D.碳酸盐难溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:

下列有关叙述正确的是
A.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
B.贝诺酯分子中有三种含氧官能团
C.乙酰水杨酸和对乙酰氨基酚均能与Na2CO3 溶液反应
D.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚
查看答案和解析>>
科目: 来源: 题型:
【题目】硼及其化合物应用广泛。回答下列问题:
(1)基态B原子的价电子轨道表达式为____________________________,其第一电离能比Be ____________(填“大”或“小”)
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是______________。

(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。
①B原子的杂化方式为_____________。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:________________________________________________________。
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸的原因是_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D四种易溶于水的白色固体,分别由Na+、Ba2+、Cu2+、Ag+、Cl-、SO42-、CO32-、NO3-中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断盐的化学式分别为:A__________;D__________。
(2)写出下列反应的离子方程式:
①B+D→:________________;③C+HCl→气体:_______________。
(3)在作实验反思时,有同学提出:如果溶液中同时存在CO32- 和Cl-,CO32- 会对Cl- 的检验产生干扰。为了确定该溶液中是否存在Cl-,该小组同学进行了如下探究实验:
 _________________________________
_________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】如图,现有芳香族化合物A,分子式为C8H8O3,含有两种官能团,A 的核磁共振氢谱存在6组峰。高聚物H不能降解,而高聚物F中含有六元环和八元环呈线性片状结构,并且可以降解。
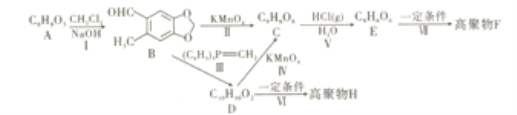
已知:①酚羟基极易被氧化;
②—CHO+(C6H5)3P=CH一R→—CH=CH—R+(C6H5)3P = O;
③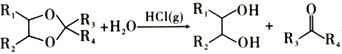 。
。
(1)化合物A中的官能团名称为_______________。反应(Ⅱ) (Ⅵ)的反应类型分别是_______________。
(2)化合物H的结构为____________________________。
(3)有同学提出可以将A 与KMnO4直接氧化反应得到E,请解释这样反应的不恰当之处。___________________________________________。
(4)反应(Ⅰ) 的化学方程式为________________________________,反应(Ⅶ) 的化学方程式为________________________________。
(5)满足下列条件的D的同分异构体有________________种。
A.含有苯环且苯环上只有两个取代基
B.含有酯基同时可以发生银镜反应
请写出核磁共振氢谱面积之比为1∶1∶2∶2∶4的化合物结构:______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com