
科目: 来源: 题型:
 右图是反应CO(g)+2H2(g)
右图是反应CO(g)+2H2(g)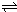 CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:阅读理解

| 9n |
| 4m |
| 9n |
| 4m |
查看答案和解析>>
科目: 来源: 题型:


| ||

查看答案和解析>>
科目: 来源: 题型:


| ||
| ||
2- 4 |
2- 4 |
查看答案和解析>>
科目: 来源: 题型:
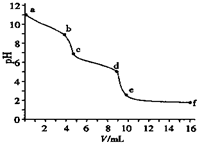 (2013?厦门二模)用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.用 pH传感器测得混合溶液的pH变化曲线如图(已知饱和CO2溶液pH为5.6),下列说法正确的是( )
(2013?厦门二模)用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.用 pH传感器测得混合溶液的pH变化曲线如图(已知饱和CO2溶液pH为5.6),下列说法正确的是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com