
科目: 来源: 题型:
【题目】工业废料和废水的处理离不开化学。
I. 某工业废料含SiO2、FeS和CuS等物质,采用如下实验方案进行回收利用。请回答下列问题:
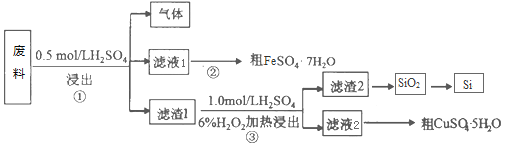
(1)已知步骤①中发生的化学反应为非氧化还原反应,写出产生气体的电子式_______,该气体可用足量的NaOH溶液吸收,该反应的离子方程式是_______________________________
(2)Si原子在周期表中的位置____________,写出晶体Si的一种主要用途___________。步骤②的操作依次为____________________、过滤、洗涤、干燥。滤渣2的主要成分是SiO2和S,写出步骤③涉及的化学方程式_________________________________。
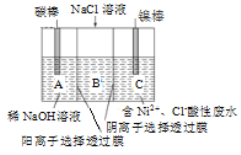
II.用一种阴、阳离子双隔膜三室电解槽处理含镍酸性废水并获得金属镍的模拟装置如图。
镍棒与外接电源____极相连。A极区电极反应式是__________________________。 电解一段时间后,B中NaCl溶液的浓度_________填“增大”、“减少”);若将图中阳离子膜去掉,将A、B两室合并,则A极区电极产物是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在“冰→液体水→氢气和氧气”的变化过程中,微粒间被破坏的作用力依次是( )
A.范德华力、范德华力
B.范德华力、共价键
C.共价键、范德华力
D.共价键、共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质在水溶液中关于电离方程式错误的是
A. MgCl2 = Mg2+ + 2Cl
B. Ba(OH)2 = Ba2+ + 2OH
C. CH3COOH = H+ + CH3COO-
D. KHSO4 = K+ + H+ + SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,将 1.0 L w mol·L-1 CH3COOH 溶液与 0.1 mol NaOH固体混合,充分反应。然后向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),溶液pH的变化如图。下列叙述正确的是
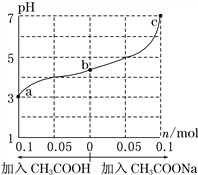
A. b点混合液中c(Na+)>c(CH3COO-)
B. 加入CH3COOH过程中,![]() 增大
增大
C. c点存在:c(CH3COOH)+c(CH3COO-) =0.1+w
D. a、b、c对应的混合液中,水的电离程度由大到小的顺序是c>a>b
查看答案和解析>>
科目: 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列说法正确的是
A. 2.3gNa在足量的氧气中充分燃烧,转移的电子数为0.2NA
B. 标准状况下,22.4 L水中含有的氧原子数为NA
C. 1L 0.5molL﹣1的AlCl3溶液中所含Cl数目为3NA
D. 0.1 mol 氯气所含有的原子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】生活中常见的荧光棒的发光原理可用下式表示:
![]() +H2O2 → 2
+H2O2 → 2![]() + 2CO2
+ 2CO2
二苯基草酸酯
上述反应产生的能量传递给荧光染料分子后,染料分子释放荧光。下列说法不正确的是
A. 可用氯化铁溶液检验上述反应有苯酚生成
B. 荧光棒发光过程涉及化学能到光能的转化
C. 二苯基草酸酯苯环上的一氯代物共有3种
D. 二苯基草酸酯与草酸二甲酯互为同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】室温时,体积为1mL、浓度均为0.1mol·L-1的两种常见物质X(OH)n、K2AO3的溶液分別加水稀释至体积为VmL,pH随lgV的变化情况如下图所示。下列叙述错误的是( )
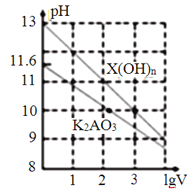
A. n=1
B. H2AO3的二级电离常数Ka2约为1.0×10-10.2
C. pH=10的两种溶液中水的电离程度相同
D. 升高温度,K2AO3溶液pH增大,X(OH)n溶液pH减小
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20 mL 0.10 mol/L甲胺的溶液中滴加0.10 mol/L盐酸时混合溶液的pH与相关微粒的浓度关系如图所示。已知:甲胺(CH3NH2)类似于氨,但碱性稍强于氨。下列说法不正确的是

A. 甲胺在水中的电离方程式CH3NH2+H2O![]() CH3NH3++OH—
CH3NH3++OH—
B. b点对应的加入盐酸的体积小于20mL
C. 将等物质的量的CH3NH2和CH3NH3Cl一起溶于蒸馏水,得到对应a点的溶液
D. 常温下,甲胺的电离常数为Kb,则pKb=—lgKb=3.4
查看答案和解析>>
科目: 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法正确的是
A. CO的摩尔质量为28g
B. 1mol·L-1 NaOH溶液中所含有Na+数目为NA
C. 8g NH4NO3中含有0.2mol N原子
D. 0.5mol H2所占的体积约为11.2L
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随加入的c(HC2O4-)的变化趋势如下图所示。下列说法正确的是( )

A. 当c(HC2O4-)=0.1mol/L时,c(H+)>c(C2O42-)-c(H2C2O4)
B. 当c(HC2O4-)>amol/L时,c(H+)< c(H2C2O4),HC2O4-的水解程度大于电离程度
C. HC2O4-![]() C2O42-+H+,Ka(HC2O4-)=a
C2O42-+H+,Ka(HC2O4-)=a
D. 将0.08mo1/L H2C2O4溶液与等浓度NaOH溶液等体积混合后(忽略体积变化),c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4)>c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com