
科目: 来源: 题型:
【题目】某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体加热,测量剩余固体的质量随时间的变化关系,如图所示。
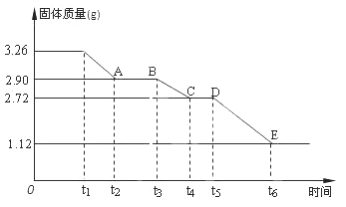
(1)t5~ t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色的气体物质的量是_______________________;
(2)x∶y=________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铁是一种重要的化学试剂,其晶体的化学式为FeCl3·6H2O。FeCl3的饱和溶液在实验室和电子工业中都有重要应用。
(1)饱和FeCl3溶液的颜色是______________色的,实验室里常用它来制备______________(化学式)胶体,具体操作方法是:先将烧杯中的水加热至沸腾,再滴入5~6滴____________________,______________至液体呈______________色,停止加热。
(2)电子工业中 ,常用FeCl3的饱和溶液来印刷电路图板,反应的原理是:Cu+2FeCl3=2FeCl2+CuCl2。该反应中______________作氧化剂,用单线桥法表示电子转移的方向和数目:____________。
(3)将0.5mol·L—1的FeCl3溶液从100mL稀释至500mL,所得溶液中,c(Cl—)为__________。(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋植物如海带和海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
某化学兴趣小组将上述流程②③设计成如下图所示操作。

已知过程②发生反应的化学方程式为Cl2+2KI===2KCl+I2
回答下列问题:
(1)写出提取过程①、③中实验操作的名称:①_____________ ③_____________
(2)四氯化碳是________色、密度比水________的液体。F中下层液体的颜色为________色,上层液体中溶质的主要成分为________。(填化学式)
(3)从F中得到固态碘还需进行的操作是___________________________。
(4)在灼烧过程中,使用到的实验仪器有(除泥三角外)_______________(填序号)。
①试管 ②瓷坩埚 ③坩埚钳 ④蒸发皿 ⑤酒精灯
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁的快速发展方便了人们的出行。工业上利用铝热反应焊接钢轨间的缝隙。反应的方程式如下:2Al+Fe2O3![]() 2Fe+Al2O3,下列说法不正确的是( )
2Fe+Al2O3,下列说法不正确的是( )
A. 氧化剂是Fe2O3,氧化产物是 Al2O3。
B. 被氧化的元素是铝,被还原的元素是铁。
C. 当转移的电子为0.3mol时,参加反应的铝为2.7g
D. Fe2O3既不是氧化剂又不是还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】锌及其化合物用途广泛。回答下列问题
(1)火法炼锌以闪锌矿(主要成分是ZnS) 为主要原料,涉及的主要反应有:
2ZnS(s)+3O2(g)=2ZnO(s)+2SO2(g) △H1=-930kJ·mol-1
C(s)+O2(g)=CO2(g) △H2=-393.5 kJ·mol-1
C(s)+CO2(g)=2CO(g) △H3= +172.5 kJ·mol-1
ZnO(s)+CO(g)=Zn(g)+CO2(g)△H4= +198 kJ·mol-1
反应ZnS(s)+tC(s)+2O2(g)=Zn(g)+CO2(g)+SO2(g)的△H =_________kJ·mol-1
(2)银锌蓄电池工作原理为Ag2O2+2Zn+2H2O![]() 2Ag +2Zn(OH)2,该蓄电池充电时,发生还原反应的物质是__________, 正极反应分为两个阶段,第二阶段为Ag2O+H2O+2e-= 2Ag+2OH-,写 出第一阶 段 正极 电极反应式_____________________________。
2Ag +2Zn(OH)2,该蓄电池充电时,发生还原反应的物质是__________, 正极反应分为两个阶段,第二阶段为Ag2O+H2O+2e-= 2Ag+2OH-,写 出第一阶 段 正极 电极反应式_____________________________。
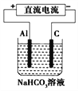
(3)以(2)中蓄电池作电源,用如图所示的装置在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是__________________(用相关的电极反应式和离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图甲是一种利用微生物将废水中的尿素(H2NCONH2)直接转化为对环境友好物质的原电池装置。现利用甲装置产生的电能对乙装置中的饱和食盐水进行电解(A、B皆为石墨电极)。下列说法中不正确的是( )

①M电极反应式:H2NCONH2+H2O+6e-=CO2↑+N2↑+6H+
②当A电极产生11.2mL气体(标况)时,则N电极消耗25×10-4mol气体
③甲中H+透过质子交换膜由右向左移动
④A电极应与X相连接
⑤反应一段时间后,乙装置U型管中的溶液pH变大
A. ①③ B. ①③⑤ C. ①②③ D. ②④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】四氯化锡用作媒染剂和有机合成上的氯化催化剂。无水四氯化锡暴露于空气中与空气中的水分反应生成白色烟雾,有强烈的刺激性气味。实验室用下列装置模拟合成四氯化锡,首先将金属锡熔融,然后泼入冷水,制成锡花,将干燥的锡花加入反应器B中,再向反应器中缓缓通入干燥氯气。
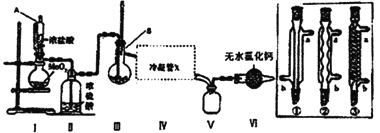
(部分夹持装置及加热仪器省略)
部分物理数据如下:
物质 | 状态 | 熔点/℃ | 沸点/℃ |
Sn | 银白色固体 | 232 | 2260 |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
回答下列问题:
(1)仪器A的名称为_____________________;Ⅳ处冷凝管应选择________________________。
(2)装置I中发生反应的离子方程式为______________________________。
(3)SnCl4在空气中与水蒸气反应生成白色SnO2·xH2O固体,其反应的化学方程式为__________________________________。
(4)该装置存在的缺陷是_________________________。
(5)下列说法正确的是__________。
A.操作中应点燃Ⅲ处酒精灯再点燃Ⅰ处酒精灯
B.用锡花代替锡粒的目的主要为了提高化学反应速率
C.该实验应该在通风橱内或在通风的地方进行
D.将产品溶于盐酸,可用溴水检测,若溴水橙色褪去,说明SnCl4中含有SnCl2
E.Ⅳ处应注意在加热之前先接通冷却水,而停止加热后,仍要继续通冷却水一段时间
(6)产品中含少量SnCl2,测定SnCl4纯度的方法:取0.200g产品溶于50mL的稀盐酸中,加入淀粉溶液作指示剂,用0.0100mol/L碘酸钾标准溶液滴定至终点,消耗标准液4.00 mL,反应原理为:3SnCl2+KIO3+6HC1=3SnCl4+KI+3H2O,判断滴定终点的依据为_____________,产品的纯度为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.在离子化合物中,可能含共价键
B.在共价化合物中,可能含离子键
C.含共价键的化合物一定是共价化合物
D.含离子键的化合物不一定是离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com