
科目: 来源: 题型:
【题目】明代宋应星著的《天工开物》中有关于“火法”冶炼锌的工艺记载:“炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。”下列说法不正确的是(注:炉甘石的主要成分为碳酸锌)
A. 该冶炼锌的反应属于置换反应
B. 煤炭中起作用的主要成分是C
C. 冶炼Zn的反应方程式为:ZnCO3+2C![]() Zn+3CO↑
Zn+3CO↑
D. 倭铅是指金属锌和铅的混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中,正确的是
A. H2SO4的摩尔质量是98
B. 等质量的O2和O3中所含的氧原子数相同
C. 等质量的CO与CO2中所含碳原子数之比为7︰11
D. 98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上接触法生产硫酸的主要反应为:SO2(g)+ ![]() O2(g)
O2(g)![]() SO3(g)。
SO3(g)。
(1)恒溫恒压下,平衡体系中SO3体积分数与SO2、O2物质的量之比的关系如图1,则b 点n(SO2)/n(O2)=_____________________。

(2)①该反应的催化剂为V2O5,其催化反应过程为:SO2+V2O5![]() SO3+V2O4 K1
SO3+V2O4 K1 ![]() O2+V2O4
O2+V2O4 ![]() V2O5 K2。则在相同温度下2SO2(g)+O2(g)
V2O5 K2。则在相同温度下2SO2(g)+O2(g) ![]() 2SO3(g)的平衡常数K=_________(以含K1、K2的代数式表示)。
2SO3(g)的平衡常数K=_________(以含K1、K2的代数式表示)。
②V2O5加快反应速率的原因______________________。
(3)某实验从废钒催化剂(主要成分为V2O5和V2O4) 中回收V2O5,其简要过程如下:

(VO2+和VO2+可看成是钒相应价态的简单阳离子完全水解的产物)
①写出水解生成VO2+的离子方程式____________________________。
②在沉钒时,为使钒元素的沉淀率达到98%,至少应调节溶液中的c(NH4+)为_________(25℃,Ksp (NH4VO3) =1.6×10-3,溶液体积变化忽略不计)
(4)在保持体系总压为0.1MPa的条件下进行反应:SO2(g)+ ![]() O2(g)
O2(g)![]() SO3(g),原料气中SO2 和O2的浓度之比(k)不同时,SO2的平衡转化率与温度(t) 的关系如图2所示:
SO3(g),原料气中SO2 和O2的浓度之比(k)不同时,SO2的平衡转化率与温度(t) 的关系如图2所示:

①图中k1、k2、k3的由大到小的顺序为____________,理由是___________________。
②图2 中A 点原料气成分为n(SO2)∶ n(O2)∶n(N2)=7∶11∶82。若反应开始时容器体积为V1,A点时容器体积为V2,则V1∶V2=_________(保留三个有效数字)
③近年,有人研发出用氧气代替空气的新工艺,使SO2趋于完全转化。此工艺的优点除了能充分利用含硫的原料外,主要还有____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列有关叙述正确的是( )
A. 24g镁在足量的O2中燃烧,转移的电子数为0.1NA
B. 分子总数为NA的NO2和CO2混合气体中含有的氧原子數为2NA
C. 1L一氧化碳气体一定比1L氧气的质量小
D. 常温常压下8gO3中含有8NA个电子
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组按下列路线合成药物奥沙拉秦:
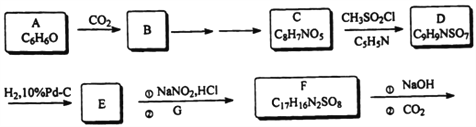
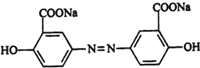 奥沙拉秦
奥沙拉秦
己知:(1)物质G是由物质B转化为物质C的一种中间产物
(2)R-NO2 ![]() R-NH2
R-NH2
(3)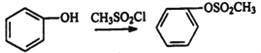
请回答:
(1)化合物A的结构简式_________________________。
(2)下列说法正确的是___________。
A.化合物A→B的反应是取代反应
B.化合物E既可以与HCl,可以与NaOH溶液反应
C.化合物F遇到FeCl3能发生显色反应
D.奥沙拉秦的分子式是C14H8N2O6Na2
(3)设计由化合物B生成化合物C的合成路线(用流程图表示,试剂任选)______________。
(4)写出C→D的化学方程式_____________________________________。
(5)化合物C可能的同分异构体的结构简式________________,须同时符合:
①1H-NMR谱表明分子中有3 种氢原子;
②IR谱显示含有苯环,N原子不与苯环直接相连接,乙酰基(CH3CO-);
③遇到FeCl3显色。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作能达到目的的是( )
A.用碱石灰干燥氯气
B.用品红溶液鉴别CO2和SO2
C.用乙醇萃取碘水中的碘单质
D.用澄清石灰水检验碳酸钠溶液中是否含有碳酸氢钠
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A.把煤粉碎了再燃烧可以提高煤的燃烧效率
B.增加炼铁高炉的高度可以降低尾气中CO的含量
C.无论加入正催化剂还是加入负催化剂都能大大提高化学反应速率
D.用完的电池可以随意地丢弃
查看答案和解析>>
科目: 来源: 题型:
【题目】已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4![]() 2AsH3↑+6ZnSO4+3H2O。
2AsH3↑+6ZnSO4+3H2O。
(1)请用双线桥法标出电子转移的方向和数目____________________________________。
(2)As2O3在上述反应中显示出来的性质是____________(填序号)。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物是__________,还原产物是________。
(4)若生成0.2 mol AsH3,则转移的电子数为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在T℃时,发生反应C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
(1)恒温时,在一个2L的密闭容器中加入4molC 和1molH2O(g),5min后反应达到平衡,C 的转化率为20%。
①0~5min 内,用H2O(g)表示的平均反应速率为_________。
②有关该反应下列说法正确的是_________。
a.容器中压强不变或混合气体密度不变均可以判定该反应已经达到平衡状态
b.若将加入的碳块改为碳粉,则能够提高水蒸气的平衡转化率
c.平衡后,再加入0 .5molC、5mol H2O(g)、2molCO、2molH2,平衡不移动
(2)已知:Ⅰ.破坏1mol 共价键所需要的能量如下表:
共价键 | 石墨中的碳碳键 | H-H | C | H-O |
能量/kJ | 475.7 | 436 | 1072 | 463 |
Ⅱ.石墨层由六角形蜂巢结构的碳原子构成,如右图所示,已知每个碳原子形成的共价键数为1.5NA。
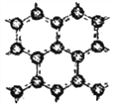
某同学构想:通过下图所示装置实现C(s)+H2O(g)![]() CO(g)+H2(g)的反应。
CO(g)+H2(g)的反应。
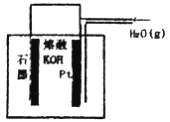
①按该考生的构想,石墨电极发生的反应式为_______________________。
②请用计算判断该构想的合理性:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com