
科目: 来源: 题型:
【题目】我国古代就有湿法炼铜的记载“曾青得铁则化为铜”,反应为Fe + CuSO4 = Cu + FeSO4。有关该反应的说法正确的是( )
A.Fe被还原B.Fe是还原剂C.CuSO4发生氧化反应D.CuSO4失去电子
查看答案和解析>>
科目: 来源: 题型:
【题目】稀土是一种重要的战略资源、氟碳铈矿主要化学成分为CeFCO3,它是提取铈等稀土元素的重要矿物原料。氟碳铈矿的冶炼工艺流程如下:
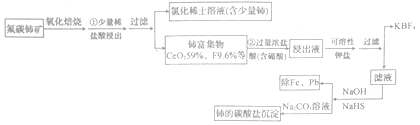
已知:Ⅰ.铈的常见化合价为+3、+4
Ⅱ.Ce4+可以与SO42-结合为[CeSO4]2+
Ⅲ. 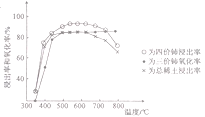
焙烧时铈被氧化成四价,四价铈不易进入溶液,而三价稀土元素易进入溶液。在盐酸浸出时,有少量铈进入滤液,且产生黄绿色气体。
回答下列问题:
(1)氟碳铈矿焙烧的目的是__________________;焙烧最适宜温度为______________(填标号)。a.350~450℃ b.550~650℃ C.750℃以上
步骤①中少量铈进入稀土溶液发生反应的离子方程式是_________________________。
(2)铈富集物用含硼酸的盐酸溶液处理,使氟转化为四氟硼酸根离子,然后用可溶性钾盐将四氟硼酸根离子转变为KBF4沉淀并过滤除去。写出生成KBF4的离子方程式:________________。此法处理铈富集物的缺点是____________________。
(3)除云氟离子后向滤液中先加入NaOH溶液,然后再加入NaHS除去铁与铅。加入NaOH溶液的目的是____________________。
(4)写出此流程中铈的碳酸盐沉淀的化学式:______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学课外兴趣小组的同学欲测定某品牌味精中食盐的含量。下面是该小组所进行的实验步骤:
①称取某品牌袋装味精样品10.0 g放入烧杯中,并加适量蒸馏水溶解;
②______________________________________;
③______________________________________;
④用蒸馏水洗涤沉淀2~3次;
⑤将沉淀烘干、称量,测得固体质量4.90 g。
根据上述实验步骤回答下列问题:
(1)请你在上面的空格内补齐所缺的实验步骤②、③。
(2)实验③所用的玻璃仪器有____________。
(3)检验沉淀是否洗净的方法是________________。
(4)若味精商标上标注:“谷氨酸钠含量≥80.0%,NaCl含量≤20.0%”,则此样品是否合格?________(填“合格”或“不合格”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某厂排出的废液主要含有硝酸锌和硝酸银,为了从中回收金属银和硝酸锌,某中学化学课外活动小组设计了以下的实验步骤:

(1)X是____________,Y是____________ (写化学式,下同)。
(2)固体A、滤液B、C的主要成分:A______________,B______________,C______________。
(3)Z处进行的操作是__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
①常温下,强酸溶液的pH=a,将溶液的体积稀释到原来10n倍,则pH=a+n;
②已知BaSO4的Ksp=c(Ba2+)c(SO42﹣),所以在BaSO4溶液中有c(Ba2+)=c(SO42﹣)=![]()
③将0.1molL﹣1的NaHS和0.1molL﹣1 Na2S溶液等体积混合,所得溶液中有c(S2﹣)+2c(OH﹣)=2c(H+)+c(HS﹣)+3c(H2S)
④在0.1mol/L氢氧化钠溶液中滴加0.1mol/L醋酸,刚好完全中和时pH=a,则由水电离产生的c(H+)=10﹣amolL﹣1.
A. ①②③④ B. 只有②③ C. 只有③④ D. 只有③
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、M、R 为周期表前四周期原子序数依次增大的五种元素,X 与其他四种元素不同周期不同主族,M原子最外层2p轨道上有两个未成对电子,Y 易与M形成两种常见的化合物,R 在周期表的第9列。回答下列问题:
(1)R 基态原子M 能层的电子排布式为_________________,其原子核外共有_________种能量的电子。
(2)Y、M均可与X形成18e-的分子,其中属于极性分子的为_____________(填化学式),分子中Y、M 两种原子杂化方式依次为___________、_________________。
(3)Z 与M可形成的两种常见酸根离子的几何构型为__________、____________。
(4)R可形成原子簇化合物R2(CO)8,其沸点为52℃,不溶于水,易溶于乙醇、苯、二硫化碳等,是一种重要的有机合成催化剂,其结构如图,则该化合物属于_________晶体,该晶体中存在的作用力有___________(填标号)。
a.离子键 b.配位键 Cσ键 d.π键 e.氢键 f.范德华力
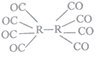
(5)单质R的晶胞有两种:417℃以下的晶胞结构如图1,417℃以上的晶胞结构如图2,后者配位数是_____________。若前者晶胞参数为ɑpm和c pm,单质R的摩尔质量为Mg·mol-1,阿伏加德罗常数为NA,则前者晶体密度p=_________g·cm-3(列出计算式即可)。

查看答案和解析>>
科目: 来源: 题型:
【题目】在室温下,同种规格的铝片分别与下列物质混合,化学反应速率最大的是( )
A.0.1mol/L的盐酸15mL
B.0.2mol/L的盐酸12mL
C.0.25mol/L的盐酸8mL
D.18mol/L的硫酸15mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com