
科目: 来源: 题型:
【题目】滴加新制氯水后,下列各组离子可能大量存在的是( )
A.Fe3+、Cl﹣、NO3﹣
B.Na+、HCO3﹣、SO42﹣
C.Ag+、NH4+、NO3﹣
D.Na+、SO32﹣、SO42﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室常用如图所示的两套装置测量所制得气体的体积,有关这两套量气装置的使用说明错误的是( )
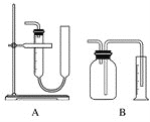
A. 量气前,B装置中广口瓶通常应盛满相应的液体
B. 使用A装置量气前,右管中应充满相应的液体
C. A装置收集完气体后,在读数前应使盛液管内的液面与集气管内的液面相平
D. A装置直接测量的是气体的体积,而B装置直接测量的是所排出液体的体积
查看答案和解析>>
科目: 来源: 题型:
【题目】室内空气污染是人类健康的“隐形杀手”,越来越受到人们关注。下列不能造成室内空气污染的是
A. 家用燃料燃烧产生的CO、CO2 B. 家庭烹调产生的油烟
C. 装饰材料散发出的甲醛、苯等 D. 保持室内空气流通
查看答案和解析>>
科目: 来源: 题型:
【题目】2017年采用中国自主知识产权的全球首套煤基乙醇工业化项目投产成功。某地煤制乙醇的过程表示如下。
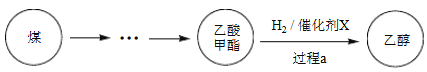
(1)Cu(NO3)2是制备“催化剂X”的重要试剂。

① 气体A是_______。
② 实验室用Cu(NO3)2固体配制溶液,常加入少量稀HNO3。运用化学平衡原理简述HNO3的作用_______。
③ NaClO溶液吸收气体A的离子方程式是_______。
(2)过程a包括以下3个主要反应:
Ⅰ.CH3COOCH3(g)+2H2(g)![]() C2H5OH(g)+CH3OH(g) ΔH1
C2H5OH(g)+CH3OH(g) ΔH1
Ⅱ.CH3COOCH3(g)+C2H5OH(g)![]() CH3COOC2H5 (g)+CH3OH(g) ΔH2
CH3COOC2H5 (g)+CH3OH(g) ΔH2
Ⅲ.CH3COOCH3(g)+H2(g)![]() CH3CHO(g)+CH3OH(g) ΔH3
CH3CHO(g)+CH3OH(g) ΔH3
相同时间内,测得CH3COOCH3转化率、乙醇和乙酸乙酯的选择性(如乙醇选择性= ![]() )如下图所示。
)如下图所示。
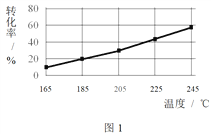
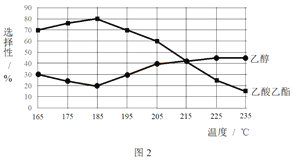
① 已知:ΔH1 < 0。随温度降低,反应Ⅰ化学平衡常数的变化趋势是_______。
② 下列说法不合理的是________。
A.温度可影响反应的选择性
B.225℃~235℃,反应Ⅰ处于平衡状态
C.增大H2的浓度,可以提高CH3COOCH3的转化率
③ 为防止“反应Ⅲ”发生,反应温度应控制的范围是_______。
④ 在185℃下,CH3COOCH3起始物质的量为5 mol,生成乙醇的物质的量是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子中,在溶液中不能大量共存的是
A. H+、Cl-、Na+、NO3- B. Ag+、NO3-、Cl-、Na+
C. Ca2+、Na+、Cl-、K+ D. Na+、H+、Cl-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组比较Cl-、Br-、I-的还原性,实验如下:
实验1 | 实验2 | 实验3 | |
装置 |
|
|
|
现象 | 试管内颜色无明显变化;用蘸浓氨水的玻璃棒靠近管口,产生白烟 | 溶液变黄;把湿润的KI淀粉试纸靠近试管口,变蓝 | 溶液变深紫色;经检验溶液含单质碘 |
下列对实验的分析不合理的是
A. 实验1中,白烟是NH4Cl
B. 根据实验1和实验2判断还原性:Br->Cl-
C. 根据实验3判断还原性:I->Br-
D. .上述实验利用了浓H2SO4的强氧化性、难挥发性等性质
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同
B. 配制一定浓度的FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度
C. 常温下,Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+溶液中,c(Mg2+)≤5.6×10-4 mol·L-1
D. 浓度为5 mol·L-1和0.5 mol·L-1的两种FeCl3溶液,其他条件相同时,Fe3+的水解程度前者比后者大
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
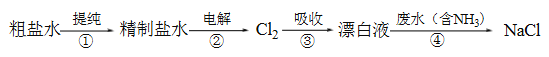
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】观察下列实验装置图,按要求作答:

(1)装置中c、d、e的名称分别为____________、____________、____________。
(2)分离下列物质,需要在哪套装置中进行?
Ⅰ.干燥H2,可采用_______(填装置序号)装置。
Ⅱ. 分离碘水中的碘应先选择装置_____(填装置序号)进行_______和_______操作。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com