
科目: 来源: 题型:
【题目】氯化亚铜(CuCl)是一种重要化工原料,难溶于水,在潮湿空气中易水解氧化。回答下列问题:
(1)CuCl的保存方法是_________。
(2)已知:Cu(s)+Cl2(g)=CuCl2(s) △H1=-218.8kJ/mol
2Cu(s)+O2(g)=2CuO(s) △H2=-310.6kJ/mol
4CuCl(s)+O2(g)=2CuCl2(s)+2CuO(s) △H5=-177.6kJ/mol
写出CuCl2分解为CuCl和Cl2反应的热化学方程式:___________。
(3)CuCl在含一定浓度Cl-溶液中会部分溶解,存在如下平衡:2CuCl(s)![]() Cu2++CuCl2- △H <0,溶液中c(Cu+)和c(CuCl2 )的关系如图。
Cu2++CuCl2- △H <0,溶液中c(Cu+)和c(CuCl2 )的关系如图。

①上述反应在B点的平衡常数K=___________。
②使图中的A点变为B点的措施可以是____________。
(4)利用CuCl难溶于水的性质,可以除去水溶液中的Cl-。
①除Cl-的方法是向含Cl-的溶液同时加入Cu和CuSO4。反应的离子方程式为_______。
②已知:Cu+Cu2+![]() 2Cu+ K =7.6×10-7;Ksp(CuCl)=2.0×10-6。通过计算说明上述除Cl-的反应能完全进行的原因____________。
2Cu+ K =7.6×10-7;Ksp(CuCl)=2.0×10-6。通过计算说明上述除Cl-的反应能完全进行的原因____________。
③若用Zn替换Cu可快除Cl-速率,但需控制溶液的pH。若pH过低,除Cl-效果下降的原因是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知: ① Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O ② SO2+SeO2+ H2O ![]() Se + SO42-+ H+
Se + SO42-+ H+
(1)依据Se与浓H2SO4的反应,写出Se和浓HNO3(还原产物为NO2)反应的化学方程式:__________________。
(2)Se与浓HNO3的反应中,氧化剂是_______, 反应中被还原的元素是_______。当有标准状况下33.6LNO2气体生成时,转移电子的物质的量是________mol。
(3)依据反应①②, 判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是__________。
(4) 配平反应②, 并用双线桥法标出电子转移的方向和数目:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各项中的物质,能满足如图中阴影部分关系的
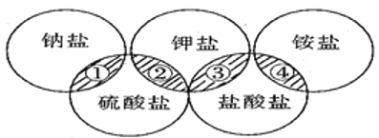
选项 | ① | ② | ③ | ④ |
A | NaCl | K2SO4 | KCl | (NH4)2SO4 |
B | NaCl | K2SO4 | KCl | NH4Cl |
C | Na2SO4 | K2SO4 | KCl | NH4Cl |
D | Na2SO4 | K2SO4 | KCl | (NH4)2SO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】以异丙苯(A)为原料合成(±)-水芹醛(C10H16O)的路线如下:

(1)(土)-水芹醛的官能团名称为______、_______。
(2)G→H反应的方程式为_____________。
(3)H→I的反应类型为_____________。
(4)B、K的结构简式分别为_____________、_____________。
(5)鉴别J和(土)一水芹醛可选用的试剂为___________。
a.NaHCO3溶液 b.溴水 c.酸性KMnO4溶液 d.新制Cu(OH)2
(6)满足下列条件的D的同分异构体有___种,其中核磁共振氢谱为1:1:2:2:6的结构简式为____。
①能与金属钠反应产生氢气;
②不能使FeCl3溶液显色;
③含有苯环且苯环上不超过两个取代基。
(7)依据题中信息,参照上述路线,以![]() 为原料,选择必要试剂设计
为原料,选择必要试剂设计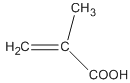 的合成路线____________。
的合成路线____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】聚氮化硫(SN)x和K3C60是两种不同类型的超导材料。回答下列问题:
(1)在基态K原子中,能量最低的空轨道的符号是_____________。
(2)S、N、K三种元素的第一电离能由大到小的顺序是____________。
(3)(SN)x具有类似黄铜的金属光泽和导电性,其结构如下图:
![]()
以S2Cl2为原料可制取(SN)x:S2Cl2→…S4N4 ![]() S2N2
S2N2 ![]() (SN)x
(SN)x
①(SN)x中N原子的杂化方式是_________;(SN)x的晶体类型是______;
②S2Cl2的结构式为________;
③Ag元素位于周期表第5周期、IB族,基态Ag原子的价电子排布式为__________。
(4)K3C60是由足球烯(C60)与金属钾反应生成的盐。
①在K3C60晶胞中,C603-堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,K+填充在空隙中。晶胞中被K+占据的空隙百分比为___________。
②C60与金刚石互为同素异形休,比较两者的熔沸点并说明理由____________。
③C60的结构是一种多面体,如图。多面体的顶点数、面数和棱边数的关系遵循欧拉定律:顶点数+面数-棱边数=2。C60分子中所含的五边形和六边形的个数分别为_____、______。

查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在恒容密闭容器中,能表示反应X(g)+2Y(g) ![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、CO32-、SO42-中的不同阳、阴离子各一种组成已知:
①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1mol/L乙溶液中c(H+)>0.1mol/L;
③向丙容器中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)甲是_____________,乙是_____________,丙是_____________,丁是_____________。
(2)50mL含Na2SO4、Na2CO3的混合溶液中加入过量的甲溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3充分反应后,沉淀减少到4.66g,并有气体产生。
①写出产生气体的离子方程式:______________________________;
②混合溶液中Na+的物质的量的浓度是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为___________,原子个数比为____________,分子的物质的量之比为__________。
(2)等温等压下,等体积的O2和O3所含分子个数比为___________,原子个数比为___________,质量比为__________。
(3)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是__________(用含NA的式子表示)。
(4)实验室中配制2mol·L—1的NaOH溶液950mL,配制时需称取的NaOH的质量是_____________。
(5)在标准状况下15gCO与CO2的混合气体,体积为11.2L混合气体的平均摩尔质量是__________;CO2与CO的体积之比是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com