
科目: 来源: 题型:
【题目】工业上可用焦炭、二氧化硅的混合物在高温下与氧气反应生成SiCl4,SiCl4经提纯后用氢气还原得高纯硅。以下是某化学小组制备干景的氧气并在实验室制备SiCl4的部分装置示意图(注: SiCl4遇水易水解)。


(1)选择上图部分装置,制备纯净干燥的氯气,正确的仪器连接顺序为:发生装置甲→___→____→_____→_____→装置A(用小写字母填空)。_____________
(2)上图C装置的作用是_______________。
(3)装置A的硬质玻璃管中二氧化硅和焦炭与氯气恰好完全反应生成SCl4,则二氧化硅和碳的物质的量之比为_________________。
(4)经过讨论,该小组认为D中吸收尾气一段时间后,除了过量的OH-,吸收液中阴离子肯定存在Cl-和SO42-,原因是__________(用离子方程式解释)。
(5)有同学认为可能还存在其它酸根离子(忽略空气中CO2的影响),提出下列假设(不考虑各因素的叠加),假设1:只有SO32-,假设2:只有ClO-,假设3:……
设计实验验证上述假设1和假设2:取少量吸收液于试管中,滴加3mol/LH2SO4至溶液呈酸性,然后将所得溶液分置于a、b两试管中,请填写空白的实验步骤、预期现象。
实验步骤(简述操作过程) | 预期現象 | 结论 |
向a试管中滴加几滴品红溶液,观察现象,加热试管a,观察到 | ____________。 ____________。 | 假设1成立 |
向b试管中滴加______________ | 溶液变为蓝色。 | 假设2成立 |
查看答案和解析>>
科目: 来源: 题型:
【题目】钴、铁、镓、砷的单质及其化合物在生产生活中有重要的应用,请回答下列问题:
(1)写出砷(As)的基态原子的电子排布式_________。
(2)N、P、As为同一主族元素,其电负性从大到小的顺序为_______,它们的简单氢化物沸点最高的是______,将NaNO2和Na2O在一定的条件下反应得到一种白色晶体,已知其中的阴离子与SO42-互为等电子体,则该阴离子的化学式为________。
(3)Fe3+、Co3+、N3+-、CN-等可形成络合离子。
①K3Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为________。
②[Co(N3)(NH3)5]SO4中Co的配位数为_______,其配离子中含有的化学健类型为_____(填离子键、共价键、配位键),C、N、O的第一电离能最大的是_____,其原因是_______。
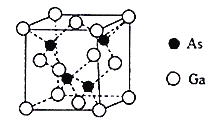
(4)砷化镓晶胞结构如图。晶跑中Ga与周围等距且最近的砷形成的空间构型为_____,已知砷化镓晶胞边长为apm,其密度为ρg·cm-3,则阿伏加德罗常数的数值为______(列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图像均为实验过程中产生沉淀的物质的量(Y)与加入试剂的量(X)之间的关系图,则其中正确的是( )


A B C D
A. 向AlCl3溶液中逐滴加入NaOH溶液至过量且边滴边振荡
B. 向NaAlO2溶液中逐滴滴加稀盐酸至过量且边滴边振荡
C. 向NH4Al(SO4)2溶液中逐滴加入NaOH溶液直至过量
D. 向等物质的量浓度的NaOH、Ba(OH)2、NaAlO2的混合溶液中逐渐通入CO2至过量
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列三个反应的化学方程式,判断有关物质的还原性的强弱顺序为( )
①I2+ SO2+ 2H2O =H2SO4+ 2HI ②2FeCl2+ Cl2= 2FeCl3
③2FeCl3+ 2HI =2FeCl2+ I2+ 2HCl
A. I-> Fe2+>Cl->SO2 B. Cl-> Fe2+> SO2>I-
C. Fe2+>I->Cl->SO2 D. SO2>I-> Fe2+>Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】符合如图所示的转化关系,且当X、Y、Z的物质的量相等时,存在焓变△H=△H1+△H2。满足上述条件的X、Y可能是

①C、CO ②S、SO2 ③Na、Na2O ④AlCl3、Al(OH)3 ⑤Fe、Fe(NO3)2 ⑥NaOH、Na2CO3
A. ①④⑤ B. ①②③ C. ①③④ D. ①③④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的鉴别方法不正确的是( )
A.用澄清石灰水鉴别SO2和CO2两种气体
B.用焰色反应鉴别NaCl和K2SO4
C.利用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液
D.用加热的方法鉴别Na2CO3和NaHCO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列试剂的保存方法错误的是( )
A.实验室少量的钠保存在煤油中
B.氢氟酸(HF)保存在无色的玻璃瓶中
C.氢氧化钠溶液保存在带橡皮塞的玻璃瓶中
D.新制的氯水保存在棕色玻璃瓶中
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
I.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H1=-41.0kJ/mol
CO2(g)+H2(g) △H1=-41.0kJ/mol
II.CO(g)+2H2(g)![]() CH3OH(g) △H2=-90.0kJ/mol
CH3OH(g) △H2=-90.0kJ/mol
III.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
回答下列问题:
(1)则△H3=______,在以上制备甲醇的两个反应中,反应II优于反应III,其原因为______。
(2)一定化例的合成气在装有催化剂的反应器中反应12小时,体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。

当温度为470K时,图中P点_____(填“是”或“不是”)处于平衡状态。490K之后,甲醇产率下降的原因是____________。
(3)图2为一定比例的CO2、H2,CO、H2,CO、CO2、.H2条件下甲醇生成速率与温度的关系。
①490K时,根据曲线a、c判断合成甲醇的反应机理是______(填“A"或“B").
A. ![]() B.
B. ![]()
②490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,结合反应I、III分析原因______________________。
(4)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的电极反应式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com