
科目: 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏伽德罗常数)
A. 地下钢铁管道用导线连接锡块可以减缓管道的腐蚀
B. 1molCl2溶于水后,溶液中Cl2、HClO、ClO-、Cl-四种粒子总数为2NA
C. 反应TiO2(s)+2Cl2(g)=TiCl4(g)△H>0能自发进行,其原因是△S>0
D. 常温下Ksp[Mg(OH)2]=5.6×10-2,则pH=10含Mg2+的溶液中,c(Mg2+)<5.6×10-8mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)某化学兴趣小组利用下列试剂:铁粉、锌粉、0.1 mol·L1 FeCl3溶液、0.1 mol·L1 FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+的氧化性、还原性,并利用实验结论解决一些问题。
①用所给试剂写出体现Fe2+具有还原性的反应的化学方程式:_________________________________。
②设计实验方案,完成下列表格。
探究内容 | 实验方案 | 实验现象 |
探究Fe3+具有氧化性 | 取少量0.1 mol·L1 FeCl3溶液,往溶液中加入足量铁粉,再加入少量KSCN溶液 | 加入铁粉后,溶液颜色变为________。加入KSCN溶液后,溶液________ |
③该兴趣小组为说明“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为_________________________________________。
(2)某反应中反应物与生成物有Fe3+、Mn2+、H+、![]() 、H2O和一种未知离子X,已知
、H2O和一种未知离子X,已知![]() 在反应中得到电子,则X离子是____________,该反应的离子方程式是____________________________。
在反应中得到电子,则X离子是____________,该反应的离子方程式是____________________________。
(3)有一铁的氧化物样品,用5 mol·L1的盐酸140 mL恰好完全溶解,所得溶液还能与通入的0.56 L氯气(标准状况)反应,使Fe2+全部转化为Fe3+,则此氧化物为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4粉末与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成。据此判断下列说法中不正确的是( )
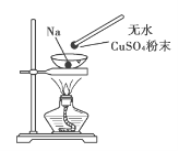
A. 上述反应是置换反应 B. 上述反应放出热量
C. 上述反应中CuSO4表现了还原性 D. 加热且无水条件下,Na可以与CuSO4反应并生成Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O
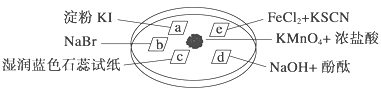
对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】海带含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
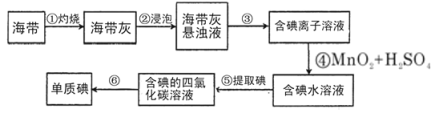
请填写下列空白:
(1)步骤③的实验操作名称是________,该操作用到的玻璃仪器有烧杯,_________,________。
(2)步骤⑤用到的玻璃仪器除烧杯外还有____________,能否用乙醇来代替CCl4________(填“能”或“否”)。
(3)步骤⑥的实验操作名称是________。
(4)步骤③得到的滤液中c(I-)=0.04mol/L,欲使用c(I-)=0.01mol/L的溶液480mL,需取用该滤液________mL。下列操作会使配制的溶液的物质的量浓度偏小的是_________。
A.稀释溶液时有液体溅出 B.容量瓶中有少量蒸馏水残留
C.取滤液时仰视刻度线 D.向容量瓶中加水定容时仰视刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应: 2A(g)+B(g) ![]() 2C(g),若经2s(秒)后测得C的浓度为0.6mol·L-1现有下列几种说法:
2C(g),若经2s(秒)后测得C的浓度为0.6mol·L-1现有下列几种说法:
①用物质A表示的反应的平均速率为0.3mol·L-1·S-1②用物质B表示的反应的平均速率为0.6mol·L-1·S-1③2s时物质A的转化率为70%④2s时物质B的浓度为0.7mol·L-1
其中正确的是( )
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】对下列平衡体系,改变条件后平衡不会正方向移动的是 ( )
A.C(s)+CO22CO(加入木炭)B.Ca(OH)2Ca2++2OH-(加入HCl)
C.H2SH++HS-(加入NaOH)D.3NO2+H2O(l)2HNO3(l)+NO(增大压强)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图制取SO2并验证SO2性质的装置图。

已知Na2SO3+H2SO4=Na2SO4+SO2+H2O。
(1)①中为紫色石蕊试液,实验现象为________,实验证明SO2是________气体。
(2)②中为红色品红溶液,现象为________证,明SO2有________性。
(3)④为紫红色高锰酸钾,实验现象为________,证明SO2有________性。
(4)⑤的作用________,反应方程式_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)下图中______(填“A”或“B”)是碱式滴定管,进行该实验的第一步操作是____________________。
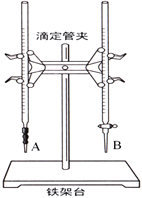
(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直到因加入一滴盐酸后,出现_____________________________(填“现象”)说明达到滴定终点。
(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是(____)
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为________mL。
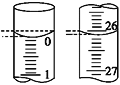
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 0.00 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 |
第三次 | 25.00 | 0.22 | 26.31 |
依据上表数据列式计算该NaOH溶液的物质的量浓度(写出简要过程)。______________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关钠的物理性质的叙述中正确的是( ) ①银白色金属;
②质软,可以用小刀切割;
③熔点低于100℃;
④密度比水小;
⑤热和电的良导体.
A.①②④
B.①②③④
C.①③④
D.①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com