
科目: 来源: 题型:
【题目】如图所示是铝箔在氧气中燃烧的实验,请回答下列问题:
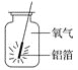
(1)铝在氧气中燃烧的化学方程式为______________________。
(2)实验时要在铝箔上系上一根火柴,其作用是______________________。
(3)集气瓶底部铺上一层细沙,其作用是______________________。
(4)实验中应观察到的现象是______________________________。
(5)用正确方法引燃铝箔,伸入装有氧气的集气瓶中后,未观察到铝箔剧烈燃烧的现象,可能的原因是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。查阅资料知:
①Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
②向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3。
③BaSO3难溶于水,可溶于稀HCl。
实验装置如图所示(省略夹持装置)
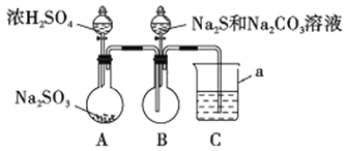
(1)仪器a的名称是_________;C中的试剂可以是______ (选填下列字母编号)。
A.稀H2SO4 B.酸性KMnO4溶液 C.饱和NaHSO3溶液 D.NaOH溶液
(2)此实验装置设计有缺陷,其改进方法是_________________________。
(3)写出B中反应的离子方程式_________________________________________。
(4)A、B中反应完后,在拆装置前,应将其中污染空气的有毒气体除去,采用的方法和具体操作是________________________________________。
(5)该法所得产品中常含有少量Na2SO3和Na2SO4。为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)
取适量产品配成稀溶液,加足量BaCl2溶液,有白色沉淀生成,_______________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(6)测定产品纯度:准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol/L碘的标准溶液滴定。(反应原理为:2S2O32-+I2=S4O62-+2I-)
①滴定至终点时,溶液颜色的变化是_______________________。
②滴定记录数据如下表:
滴定前读数/mL | 滴定后读数/mL | |
第一次 | 0.10 | 16.12 |
第二次 | 1.10 | 17.08 |
第三次 | 1.45 | 19.45 |
第四次 | 0.00 | 16.00 |
③产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室只有36.5%(d=1.19)的浓盐酸,现需配制100 mL 10%(d=1.08)的盐酸,需36.5%的浓盐酸________mL。在配制过程中,用到的仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要______。定容时,如果眼睛仰视刻线,配制的溶液的浓度将__________(填“偏高”“偏低”或“无影响”),10%的盐酸逐滴加入到纯碱溶液中,反应的离子方程式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】1mol H2燃烧生成液态水时放出285.8kJ 热量,下列表示该反应的热化学方程式正确的是
A. 2H2(g)+O2(g)=2H2O(l) △H =-142.9kJ/mol
B. 2H2(g)+O2(g)=2H2O(l) △H =+571.6 kJ/mol
C. 2H2(g)+O2(g)=2H2O(l) △H =-57l.6 kJ/mol
D. 2H2+O2=2H2O △H =-571.6kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】用硫及其化合物制硫酸有下列三种反应途径,某些反应条件和产物已省略。下列有关说法不正确的是( )
途径①:S![]() H2SO4
H2SO4
途径②:S![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
途径③:FeS2![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
A. 途径①的反应中体现了浓硝酸的强氧化性
B. 途径②、③的第二步反应在实际生产中可以通过增大氧气的浓度来降低成本
C. 由途径①、②、③分别制取1 mol 硫酸,理论上各消耗1 mol 硫,各转移6 mol 电子
D. 途径②、③比途径①污染相对小且原子利用率高
查看答案和解析>>
科目: 来源: 题型:
【题目】下列元素中,基态原子的价层电子排布式不正确的是( )
A. As 4s24p3 B. Cr 3d44s2 C. Ga 4s24p1 D. Ni 3d84s2
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,二元弱酸H2A溶液中滴加NaOH溶液,所得混合溶液pH与离子浓度变化如图所示,下列说法正确的是( )

A. 直线M表示pH与lg![]() 的变化关系
的变化关系
B. Ka2(H2A)=10-4.3
C. 交点e的溶液中:c(H2A)=c(A2-)>c(HA-)>c(H+)>c(OH-)
D. f点溶液中:c(H+)-c(OH-)=c(HA-)+c(A2-)-c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com