
科目: 来源: 题型:
【题目】已知有以下物质相互转化。试回答:
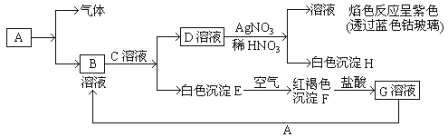
(1)写出B的化学式_____________________D的化学式________________。
(2)写出由E转变成F的化学方程式_____________________________________。
(3)写出用KSCN鉴别G溶液的离子方程式____________________________;向G溶液加入A的有关离子反应方程式________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,几种弱酸的电离平衡常数如下表所示,下列说法正确的是
化学式 | HCOOH | H2CO3 | HCN |
电离平衡常数 | K=1.8×10-4 | K1=4.3×10-7 K2=5.6×10-11 | K=4.9×10-10 |
A. H2CO3溶液和NaCN溶液反应的离子方程式为H2CO3+CN-==HCO3-+HCN
B. HCOOH的电离平衡常数表达式为K= c(HCOOH)/[c(HCOO-)·c(H+)]
C. Na2CO3溶液显碱性,NaHCO3溶液显酸性
D. 酸性强弱顺序是HCOOH>HCN>H2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:__________________________。
(2)小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_________________。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与金属铜发生反应的离子方程式:_________________________________。
(4)除去Na2CO3粉末中混入的NaHCO3杂质最佳方法是_________,化学方程式为________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于反应KClO3+6HCl=KCl+3Cl2↑+2H2O的说法不正确的是
A. KClO3是氧化剂 B. KCl既不是氧化产物也不是还原产物
C. HCl是还原剂 D. 每生成1molCl2消耗还原剂的物质的量为2 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】碲(Te)是一种第VIA族分散稀有元素,主要伴生于铜、镍、铅等金属矿藏中。TeO2属于两性氧化物,难溶于水,易溶于强酸和强碱。工业上可从电解精炼铜的阳极泥(主要成分Cu2Te,还有少量的Ag、Au)中提取碲。其工艺流程如下:
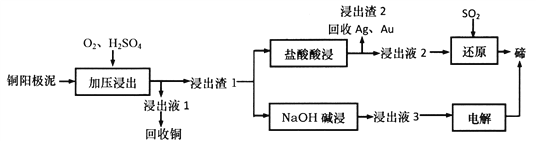
(1)“加压浸出”生成TeO2的离子方程式为________________________,“加压浸出”时控制pH为4.5~5.0,酸性不能过强的原因是_________________________________。
(2)“盐酸酸浸”后将SO2通入浸出液即可得到单质碲,该反应中氧化剂与还原剂物质的量之比为________________,该流程中可循环利用的物质是_____________(填化学式)。
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgC1)=1.80×10-10。盐酸酸浸时,“浸出渣1”中Ag2SO4可充分转化为AgC1。通过计算说明为什么可以实现充分转化_________________。
(4)NaOH碱浸时反应的离子方程式为__________________。流程中,电解过程用石墨为电极得到碲,阴极的电极反应式为__________________________________。
(5)浸出法是工业提取金属常用的方法,某实验小组用1.0mol· L-1的草酸在75℃时浸出镍。随时间变化,不同固液比对镍浸出率的影响曲线如图所示。
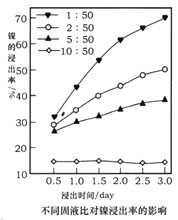
①由图可知,固液比与镍浸出率的关系是______________________。
②除固液比之外,你认为影响金属浸出率的因素还有____________________(至少两项)。
查看答案和解析>>
科目: 来源: 题型:
【题目】C1O2作为一种强氧化剂,是国际上公认的高效消毒灭菌剂,但因其易爆有毒,常用NaClO2替代。常温下,将NaOH固体加入到由0.1molC1O2溶于水配成的1L溶液中。溶液pH及部分组分含量变化曲线如图,下列叙述不正确的是

(已知:2C1O2+H2O![]() HC1O2+H++C1O3-)
HC1O2+H++C1O3-)
A. Ka(HClO2)≈10-4.5
B. 不能用pH试纸测该溶液的pH
C. 酸性:HClO2<HClO3,氧化性:HClO2>HClO3
D. 该图像上任何一点,都有c(C1O2-)+c(HC1O2)+c(C1O3-)=0.1mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】关于Na2CO3与NaHCO3的性质判断正确的是
A. 常温下溶解度:Na2CO3<NaHCO3
B. 热稳定性:Na2CO3<NaHCO3
C. 与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3
D. 与澄清石灰水反应,均有白色沉淀生成
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,既是化合反应,又是氧化还原反应的是
A. 生石灰与水反应:CaO+ H2O =Ca(OH)2
B. 氯气通入溴化钠溶液:C12+2NaBr= 2NaCl+Br2
C. 铁和氯气反应:2Fe+3Cl2![]() 2FeC13
2FeC13
D. 氯化钠溶液和浓硫酸混合加热:2NaCl+H2SO4(浓)![]() Na2SO4+2HCl↑
Na2SO4+2HCl↑
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示AE五种物质间的相互转化关系,其中A为淡黄色固体,B为单质。试推出各物质的化学式,并写出B→C、C→D、D→E反应的化学方程式。
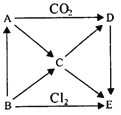
(1)写出B→C、C→D、D→E反应的化学方程式:
B→C:_______________;
C→D:_______________;
D→E:_______________;
(2)将3.9 gA投入到足量的水中充分反应,生成的气体在标准状况下的体积为_____L,将反应后的溶液配成1000mL溶液,所得溶液的物质的避浓度为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2017年3月21日是第二十五届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品1L,进行了三组实验,其操作和有关图像如下所示:

请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的阴离子是__________,一定存在的阳离子是___________。
(2)写出实验③图像中沉淀达到最大量且质量不再发生变化阶段发生反应的离子反应方程式:________。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为______,所得沉淀的最大质量是______g。
(4)若通过实验确定原废水中c(Na+)=0.18 mol·L-1,试判断原废水中NO3-是否存在?____(填“存在”“不存在”或“不确定”)。若存在, c(NO3-) = _____ mol·L-1。(若不存在或不确定则此空不填)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com