
科目: 来源: 题型:
【题目】有资料显示过量的氨气和氯气在常温下可合成岩脑砂(主要成分为NH4Cl),某实验小组对该反应进行探究,并对岩脑砂进行元素测定。
(1)岩脑砂的制备

①写出装置B中反应的化学方程式:_____________________________。
②装置C的仪器名称是_____________,装置F的作用是______________________。
③为了使氨气和氯(在D中充分混合,上述装置的合理连接顺序:_______→e f←_______(用小写字母和箭头表示,箭头方向与气流方向一致)。
④证明氨气和氯气反应有NH4Cl生成,需要的检验试剂中除了蒸馏水、稀硝酸、硝酸银溶液、红色石蕊试纸外,还需要_______________________。
(2)岩脑砂中元素的测定
准确称取ag岩脑砂,与足量的氧化铜混合加热
(发生的反应为:2NH4Cl+3CuO![]() 3Cu+N2↑+2HC1+3H2O),利用下列装置测定岩脑砂中氮元素和氯元素的物质的量之比。
3Cu+N2↑+2HC1+3H2O),利用下列装置测定岩脑砂中氮元素和氯元素的物质的量之比。

①装置H中盛装的试剂是_____________,其作用是_____________________。
②若装置I增重bg,利用装置K测得气体体积为V L(已知常温常压下气体摩尔体积为24.5L·mol-l),则岩脑砂中n(N)∶n(Cl)=_________(用含b、V 的代数式表示,不必化简)
③若取消J装置(其它装置均正确),n(N)∶n(Cl)比正常值________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中碳酸钠的质量分数。
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。则坩埚中发生反应的化学方程式为____________________________。
[方案二]称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量氢氧化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-=BaCO3↓+H2O)。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为__________。
(2)实验中判断沉淀是否完全的方法是_________________________。
[方案三]按如下图所示装置进行实验:
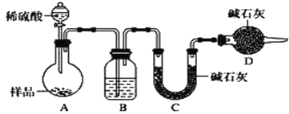
(1)D装置的作用是______________________,分液漏斗中__________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80 g,则样品中碳酸钠的质量分数为_____。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.10 mol·L-1HCl溶液滴定20 mL 0.050 mol·L-1Na2CO3和0.025 mol·L-1NaHCO3混合溶液,得出如图所示的滴定曲线。下列说法不正确的是
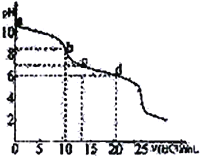
A. a点溶液显碱性的主要原因:CO32-+H2O![]() HCO3-+CH-
HCO3-+CH-
B. b点溶液中:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. c点溶液中:c(Na+)=c(HCO3-)+2c(CO32-)+ c(Cl-)
D. d点溶液中:c(Na+)> c(Cl-)> c(HCO3-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。

填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的是________,A中反应的离子方程式是________。
(2)实验开始时应先将活塞a打开,其目的是____________________。
(3)简述生成Fe(OH)2的操作过程:_______________________
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为____。
(5)图中________(填“能”或“不能”)较长时间看到Fe(OH)2白色沉淀。
查看答案和解析>>
科目: 来源: 题型:
【题目】短用期元素W、X、Y、Z的原子序数依次增大,a、b、c、d 是由W、X、Z这三种元素组成的二元化合物,其中a、c具有漂白性;e是元素Z形成的黄色固体单质;X与Z位于同主族;Y是同周期中原子半径最大的元素。上述物质在常温下的转化关系如图所示,下列说法不正确的是

A. X、Y 形成的简单离子的半径大小:X<Y
B. Z的最高价氧化物的水化物为强酸
C. a、b和c两两之间均能发生化学反应
D. Y与Z形成的化合物溶于水可促进水的电离
查看答案和解析>>
科目: 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯(ClO2)气体,该反应的化学方程式为2KClO3+4HCl(浓) === 2KCl + 2ClO2↑+ Cl2↑+ 2H2O。
(1)该反应中还原产物与氧化产物的物质的量之比为_________________。
(2)若该反应中有490克KClO3参加反应,则被氧化的HCl的质量为______________。
(3)若该反应产生2.24L(标准状况)ClO2,则转移的电子数目为_____________。
(4)某地生产的食盐氯化钠中含有少量的剧毒物质氰化钠(NaCN),用ClO2可除去其中的氰化钠,从而得到纯净的食盐,同时产生两种无毒气体。写出该反应的化学方程式: ______________________。
(5)用双线桥法表示下列氧化还原反应的电子转移情况:____________________
2KClO3+4HCl(浓) === 2KCl + 2ClO2↑+ Cl2↑+ 2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,A、B、C、D为石墨电极,E、F分别为短周期相邻两种活泼金属中的一种,且E能与NaOH溶液反应。按图示接通线路,反应一段时间。
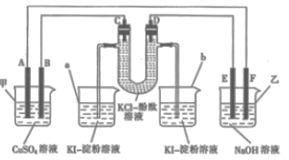
(1)甲池是________(填“原电池”或“电解池”,下同)装置;乙池是________装置。
(2)C极为________(填“阴极”或“阳极”)。
(3)烧杯中溶液会变蓝的是_________________(填“a”或“b”)。
(4)C极上的电极反应式为___________________________________。
(5)甲池中反应的化学方程式为______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种Cu- Li可充电电池的工作原理如图所示,其中非水系电解液和水系电解液被锂离子固体电解质陶瓷片( LISICON)隔开。下列说法正确的是
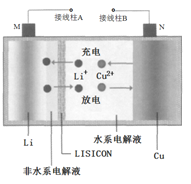
A. 陶瓷片允许水分子通过
B. 电池放电时,N极上发生氧化反应
C. 电池充电时,接线柱B应与外接直流电源的负极相连
D. 电池充电时,阴极反应为Li++e-=Li
查看答案和解析>>
科目: 来源: 题型:
【题目】某二元酸(H2A)在水中的电离方程式是H2A=H++HA-,HA-![]() H++A2-。
H++A2-。
(1)Na2A溶液显_________(填“酸性”“中性”或“碱性”)。理由是__________(用离子方程式表示)。
(2)已知0.1mol/L的NaHA溶液的pH=2,则0.1mol/L的H2A溶液中c(H+ )_______(填“<”“>”或“=”)0.11mol/L。
(3)在0.1mol/L的Na2A溶液中,下列微粒浓度关系式不正确的是__(填字母)。
A.c(A2- )+c(HA-)=0.1mol/L
B.c(OH-)=c(H+) +c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
(4)若向0.1mol/L的H2A溶液中加入等体积等浓度的NaOH溶液,则溶液中各离子浓度由大到小的顺序为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com