
科目: 来源: 题型:
【题目】下列实验装置(部分仪器已省略)或操作,能达到相应实验目的的是
A. 闻气体气味 B. 干燥氯气
B. 干燥氯气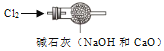
C. 分离乙醇和水 D. 配制100 mL 0.10 molL﹣1盐酸
D. 配制100 mL 0.10 molL﹣1盐酸
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中进行下列反应 CO2(g) + C(s)![]() 2CO(g) △H >0 达到平衡后,改变下列条件,分析指定物质的浓度及平衡如何变化:
2CO(g) △H >0 达到平衡后,改变下列条件,分析指定物质的浓度及平衡如何变化:
(1)增加C的量 ,平衡______________(填“向正反应方向移动”或“向逆反应方向移动”或“不移动” ;下同),c(CO)_______ (填“增大”或“减小”或“不变”;下同)
(2)减小密闭容器的体积,保持温度不变, 则平衡_____________,c(CO2)________。
(3)通入N2,保持密闭容器体积和温度不变, 则平衡___________,c(CO2)________。
(4)保持密闭容器体积不变,升高温度, 则平衡______________, c(CO)_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为研究铁盐与亚硫酸盐之间的反应,某研究小组利用孔穴板进行了实验探究:
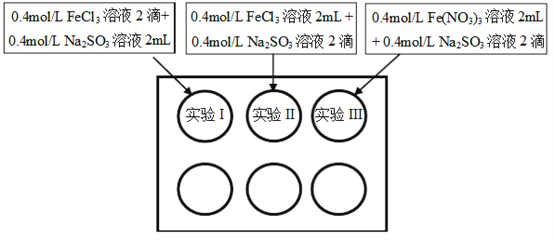
小组记录的实验现象如下表所示:
开始时 | 5min后 | 3天后 | |
实验I | 溶液立即变为红褐色,比II、III中略浅 | 与开始混合时一致 | 溶液呈黄色,底部出现红褐色沉淀 |
实验II | 溶液立即变为红褐色 | 红褐色明显变浅 | 溶液呈黄绿色 |
实验III | 溶液立即变为红褐色 | 红褐色变浅,比II中深 | 溶液呈黄色 |
(1)测得实验所用0.4mol/L FeCl3溶液及Fe(NO3)3溶液pH均约为1.0。两溶液均呈酸性的原因是__________(用离子方程式表示)。
(2)开始混合时,实验I中红褐色比II、III中略浅的原因是___________。
(3)为了探究5min后实验II、III中溶液红褐色变浅的原因,小组同学设计了实验IV:分别取少量5min后实验I、II、III中溶液,加入2滴铁氰化钾溶液,发现实验II、III中出现蓝色沉淀,实验I中无明显变化。根据实验IV的现象,结合化学用语解释红褐色变浅的原因是___________。
(4)针对5min后实验III中溶液颜色比实验II中深,小组同学认为可能存在三种因素:
①Cl- 可以加快Fe3+与SO32-的氧化还原反应;
②___________;
③NO3- 在酸性环境下代替Fe3+氧化了SO32-,同时消耗H+,使Fe3+水解出的Fe(OH)3较多。
通过实验V和实验VI进行因素探究:
实验操作(已知Na+对实验无影响) | 5min后的现象 | |
实验V | 在2mL pH=1.0的0.4mol/L Fe(NO3)3溶液中溶解约___________固体,再加入2滴0.4mol/L Na2SO3溶液 | 溶液的红褐色介于II、III之间 |
实验VI | 在2mL pH=1.0的稀硝酸中溶解约0.19g NaNO3固体,再加入2滴0.4mol/L Na2SO3溶液。向其中滴入少量BaCl2溶液 | _____________ |
实验结论:因素①和因素②均成立,因素③不明显。请将上述方案填写完整。
(5)通过上述实验,以下结果或推论合理的是___________(填字母)。
a.Fe3+与SO32-同时发生水解反应和氧化还原反应,且水解反应的速率快,等待足够长时间后,将以氧化还原反应为主
b.浓度为1.2 mol/L的稀硝酸在5min内不能将Fe2+氧化
c.向pH大于1的稀硝酸中加入少量Ba(NO3)2,使其完全溶解,可用来检验实验I的上层清液中是否存在SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】四氧化三锰(Mn3O4)是电子工业的磁性材料,而氯化铅(PbCl2)常用于焊料和助溶剂、制备其他铅盐等。用方铅矿精矿(主要成分为PbS)和软锰矿(主要成分是MnO2,还含有Fe2O3、Al2O3等杂质)制备PbCl2和Mn3O4的工艺流程如下:

已知:PbCl2(s) + 2Cl-(aq) ![]() PbCl42- ( aq) ΔH > 0
PbCl42- ( aq) ΔH > 0
(1)80℃时,为提高方铅矿精矿、软锰矿与盐酸反应的速率,可采取的措施有________(写出一条即可)。
(2)试剂X是___________。(填“化学式”)
(3)用盐酸处理两种矿石粉末,生成MnCl2、PbCl2和S的总反应化学方程式为___________。
(4)结合化学用语回答,向酸浸液中加入饱和食盐水的目的是___________。
(5)向滤液b中通入NH3和O2发生反应后,总反应的离子方程式为___________。
(6)金属锰可以用Mn3O4为原料,通过铝热反应来制备,当生成5.5 kg Mn 时,理论上消耗金属铝的质量最少为___________kg。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中各微粒的浓度关系不正确的是( )
A. 0.1 mol·L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B. 1 L浓度均为 0.1 mol·L-1 CuSO4、(NH4)2SO4的混合溶液中:c(SO![]() )>c(NH)>c(Cu2+)>c(H+)>c(OH-)
)>c(NH)>c(Cu2+)>c(H+)>c(OH-)
C. 0.1 mol·L-1 NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO![]() )+c(OH-)
)+c(OH-)
D. 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A. 95℃纯水的pH<7,说明加热可导致水呈酸性
B. pH=3的醋酸溶液,稀释至10倍后pH=4
C. 0.2mol/L的盐酸,与等体积水混合后pH=1
D. pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,a、b、c、d均为石墨电极,通电进行电解。下列说法正确的是( )
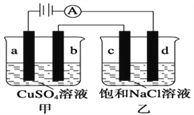
A. 乙烧杯中d的电极反应为 2Cl––2e– =Cl2↑
B. a、c两极产生气体的物质的量相等
C. 乙烧杯中发生的反应为2NaCl + 2H2O![]() 2NaOH + H2↑+ Cl2↑
2NaOH + H2↑+ Cl2↑
D. 甲、乙两烧杯中溶液的pH均保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在1×105 Pa,298 K条件下,2mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A. H2O(g) = H2(g) + ![]() O2 (g) △H = +242 kJ/mol
O2 (g) △H = +242 kJ/mol
B. 2H2(g) + O2 (g) = 2H2O (l) △H = -484 kJ/mol
C. H2 (g) + ![]() O2 (g) = H2O (l) △H = -242 kJ/mol
O2 (g) = H2O (l) △H = -242 kJ/mol
D. 2H2 (g) + O2 (g) = 2H2O (g) △H = +484 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学用语表示正确的是
A. 硫酸亚铁的电离方程式:Fe2(SO4)3 =2Fe3++3SO42-
B. H2SO4的电离方程式:H2SO4=H2+ + SO42-
C. 质子数为6,中子数为7的微粒:76C
D. 钠离子的结构示意图:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com