
科目: 来源: 题型:
【题目】下列说法正确的是
A. 高级脂肪酸乙酯的碱性水解属于皂化反应
B. 蔗糖、淀粉、纤维素均为高分子化合物
C. 硫酸铜溶液可使蛋白质变性,可用于游泳池的杀菌消毒
D. 氨基酸分子中都含有-NO2 和-COOH
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 纳米材料是指一种称为“纳米”的新物质制成的材料
B. 复合材料有强度高、质量轻、耐高温、耐腐蚀等性能,其综合性质超过单一材料
C. 光导纤维是以二氧化硅为主要原料制成的
D. 合成纤维的主要原料是石油、天然气、煤等
查看答案和解析>>
科目: 来源: 题型:
【题目】最近,科学家冶炼出了纯度高达99、9999%的铁,你估计它不会具有的性质是
A. 硬度比生铁高 B. 在潮湿的空气中放置不易生锈
C. 与4mol/L盐酸的反应生成氢气 D. 在冷的浓H2SO4溶液中可钝化
查看答案和解析>>
科目: 来源: 题型:
【题目】下面有关各种形态的能量的相互转换途径叙述,错误的是( )
A.家庭液化气灶将化学能转变为热能
B.灯泡将电能全部转变为热能
C.光合作用,将光能转变为化学能
D.太阳能电池将光能转变为电能
查看答案和解析>>
科目: 来源: 题型:
【题目】Ca10(PO4)6(OH)2(羟基磷酸钙,简写HAP)是一种新型的环境功能矿物材料,可用于除去水体中的F-、Cd2+、Pb2+及Cu2+等。
(1)制备HAP的步骤如下:分别配制250mL浓度均为0.5 mol·L-1的Ca(NO3)2溶液和(NH4)2HPO4溶液(pH约为8),按n(Ca)/n(P)=1.67分别量取相应体积的溶液,加热至50℃,不断搅拌下,按特定的方式加料,强力搅拌1h,再经后续处理得到产品。
①特定的加料方式是__________ (填序号)。
a.将Ca(NO3)2溶液逐滴滴入(NH4)2HPO4溶液中,再用氨水调节pH至10.5
b.将(NH4)2HPO4溶液逐滴滴入Ca(NO3)2溶液中,再用氨水调节pH至10.5
c.将(NH4)2HPO4溶液和氨水混合并调节pH至10.5,再滴入Ca(NO3)2溶液
②反应生成Ca10(PO4)6(OH)2的离子方程式为__________。
(2)HAP脱除F-的操作是:在聚四氟乙烯烧杯中加入50mL10mg·L-1NaF溶液和0.15gCa10(PO4)6(OH)2,在恒温下振荡,每隔1h测定一次溶液中F-浓度,直至达到吸附平衡。
①实验中“烧杯”材质用“聚四氟乙烯”塑料而不用玻璃,其原因是__________。
②除氟反应形式之一是:Ca10(PO4)6(OH)2+20F-![]() 10CaF2+6PO43-+2OH-,该反应的平衡常数K=__________[用Ksp(CaF2)和Ksp(HAP)表示]。
10CaF2+6PO43-+2OH-,该反应的平衡常数K=__________[用Ksp(CaF2)和Ksp(HAP)表示]。
(3)HAP脱除Pb(Ⅱ)包括物理吸附和溶解-沉淀吸附。物理吸附时,HAP的特定位可吸附溶液中某些阳离子;溶解-沉淀吸附的机理为:
Ca10(PO4)6(OH)2(s)+2H+(aq)![]() 10Ca2+(aq)+6PO43-(aq)+2H2O(l)(溶解)
10Ca2+(aq)+6PO43-(aq)+2H2O(l)(溶解)
10Pb2+(aq)+6PO43-(aq)+2H2O(l)![]() Pb10(PO4)6(OH)2(s)+2H+(aq)(沉淀)
Pb10(PO4)6(OH)2(s)+2H+(aq)(沉淀)
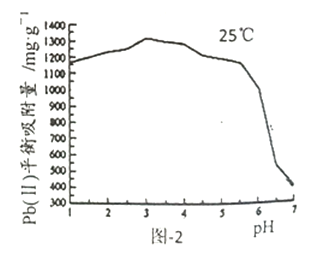
已知Pb(Ⅱ)的分布分数如图-1所示;一定条件下HAP对Pb(1)平衡吸附量与pH的关系如图-2所示。
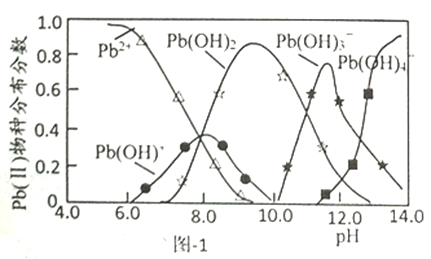
①能使甲基橙显红色的Pb(Ⅱ)溶液中滴入少量NaOH至溶液呈中性,该过程中主要反应的离子方程式为__________。
②当pH<3.0时,pH越小HAP对Pb(Ⅱ)平衡吸附量稍减小,其原因是__________。
③当pH>7.0时,生成的沉淀为__________(填化学式);此时pH越大HAP对Pb(Ⅱ)平衡吸附量越小,其原因是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 1mol/L的NaCl溶液中含有NA个Na+和NA个Cl-
B. 常温常压下,32g的O2和O3混合气体中含有的分子数为2NA
C. 由“CO(g)+2H2(g) ![]() CH3OH(g) ΔH=-129.0kJ/mol”可知:因为该反应是可逆反应,所以每消耗2NA个H2分子时反应放出的热量小于129.0 kJ
CH3OH(g) ΔH=-129.0kJ/mol”可知:因为该反应是可逆反应,所以每消耗2NA个H2分子时反应放出的热量小于129.0 kJ
D. 1L 0.1 mol/L (NH4)2SO4溶液中含N原子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作不正确的是
A.  实验室中制取少量的乙酸乙酯 B.
实验室中制取少量的乙酸乙酯 B.  比较硫、碳、硅三种元素的非金属性强弱
比较硫、碳、硅三种元素的非金属性强弱
C.  处理尾气 D.
处理尾气 D.  测定黄铜(Cu、Zn合金)中的Zn含量
测定黄铜(Cu、Zn合金)中的Zn含量
查看答案和解析>>
科目: 来源: 题型:
【题目】向500 mL NaOH溶液中投入10.8 g Al,二者恰好完全反应,请计算:
(1)Al的物质的量。
(2)参加反应的NaOH的物质的量和原溶液中溶质的物质的量浓度。
(3)在标准状况下生成H2的体积。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)1.8g H2O中有______个氧原子
(2)标况下11.2L CH4的物质的量为______mol,质量为_________;
(3)配制90mL 2.00 mol·L-1 NaCl溶液需要NaCl固体的质量是________g;
查看答案和解析>>
科目: 来源: 题型:
【题目】用废雷尼镍(主要成分为NiO、Al,少量Cr、Fe、C、S及有机物)制备Ni(NO3)2·6H2O的实验流程如下:
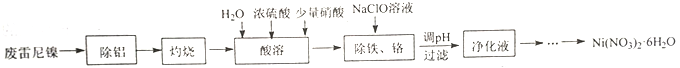
已知:①在实验条件下,Ni2+、Cr3+在溶液中不能被NaClO或HNO3氧化。
②NiSO4易溶于水,NiCO3难溶于水;Ni(NO3)2在20℃、90℃时溶解度依次为79.2、188g/100g水。
③己知“酸溶”后的溶液中主要的四种离子开始沉淀与沉淀完全的pH如下:
Ni2+ | Fe2+ | Fe3+ | Cr3+ | |
开始沉淀pH | 6.2 | 7.6 | 2.3 | 4.5 |
沉淀完全pH | 8.5 | 9.1 | 3.3 | 5.6 |
(1)“除铝”所用试剂及主要操作为__________。
(2)“灼烧”的主要目的是__________。
(3)“酸溶”时,用浓硫酸和水代替稀硫酸的目的是__________。
(4)“除铁、铬”时,Fe2+被氧化为Fe3+的离子方程式为__________;氧化后需将溶液pH调整到的范围是__________。
(5)请设计由“净化液”制取Ni(NO3)2·6H2O的实验方案:__________,离心分离、洗涤、干燥得Ni(NO3)2·6H2O (实验中须使用的试剂有:6mol·L-1硝酸,3 mol·L-1Na2CO3溶液)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com