
科目: 来源: 题型:
【题目】硒是制造光电池的一种原料,人体缺少硒就会得“克山病”。从电解精炼铜的阳极泥中提取硒的流程如下,已知阳极泥中硒以Se、Ag2Se、Cu2Se等形式存在:

请回答下列问题:
(1)电解精炼铜时,粗铜与电源的_____(填“正极”或“负极”)相连。
(2)SeO2溶于水得到H2SeO3(Ka1=3.5×10-3,Ka2=5.0×10-8),常温下亚硒酸溶液与少量氢氧化钠溶液反应的离子方程式为:_________________,反应所得的盐形成的溶液pH____7,(填>、<或=)原因是________________________________(用相关数据及必要的文字说明)
(3)亚硒酸溶液与SO2反应制硒的化学方程式为_____________________________。电解亚硒酸溶液可制得强酸H2SeO4,则电解时的阴极反应式为________________。
(4)上述硒的提取过程中除了焙烧过程中浓硫酸有强烈的腐蚀性外,还存在的主要问题是___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A. 甲苯与足量H2加成产物的一氯取代物有5种
B. ![]() 由3种单体加聚得到
由3种单体加聚得到
C. 双糖、多糖在稀酸的催化下最终均水解为葡萄糖
D. 分子式为C4H6O2并能与饱和NaHCO3溶液反应生成CO2的有机物有3种(不含立体异构)
查看答案和解析>>
科目: 来源: 题型:
【题目】相对分子质量不超过100的有机物A,既能与金属钠反应产生无色气体,又能与碳酸钠反应产生无色气体,还可以使溴的四氯化碳溶液褪色。 A完全燃烧只生成CO2和H2O。经分析其含氧元素的质量分数为37.21%。
(1)其A相对分子质量为__________________。
(2)经核磁共振检测发现A的图谱如下:

试写出A可能的结构简式:_______________________________。
(3)试写出A与甲醇反应生成有机物B的化学反应方程式:_________________。
(4)B在一定条件下可以反应生成有机玻璃(聚合物),写出反应的方程式:____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(一)某化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。
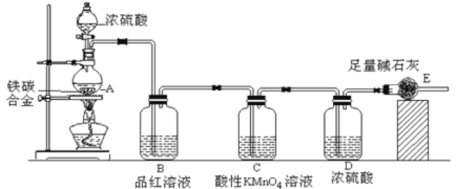
(1)仪器A的名称是___________。
(2)C装置的作用______________。
(3)该小组同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能会导致铁质量分数测量值偏低的是___________。
A.A中反应不完全
B.反应生成的SO2部分被E中碱石灰吸收
C.E中碱石灰会吸收空气中的CO2和H2O
D.反应完全后,还有CO2气体滞留在装置体系中
(二)将19.20 g CuO和Fe2O3的混合物在高温下与足量的CO充分反应,反应后全部气体用200 mL 1.20 molL-1 Ba(OH)2溶液吸收,生成35.46 g白色沉淀(不考虑沉淀的溶解,忽略溶液体积的变化)。
(4)则吸收气体后溶液中溶质的化学式为________,其浓度为_________。
(5)混合物中CuO和Fe2O3的物质的量之比为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.若已知: Cu(OH)2 (s) ![]() Cu2+ (aq)+2OH—(aq) △H= akJ/mol
Cu2+ (aq)+2OH—(aq) △H= akJ/mol
H2O(l) ![]() H+(aq) + OH—(aq) △H= bkJ/mol
H+(aq) + OH—(aq) △H= bkJ/mol
请写出Cu2+发生水解反应的热化学方程式________________________________,该反应的平衡常数为_______,已知:25℃时, Ksp[Cu(OH)2]=2.0×10-20 mol3/L3
II.室温下,现有①0. 2 mol/L NaOH溶液、②0.2 mol/L HX溶液,两溶液等体积混合后,测得溶液pH=8则:
(1)上述混合液中各离子浓度由大到小的顺序为_______________________
(2)pH=12的NaOH溶液与pH=2的HX等体积混合,混合后溶液显______性(填“酸”、“碱”或“中”)。
III. NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图。

该电池在使用过程中正极反应为:O2+4e-+2N2O5=4NO3—,石墨I电极上生成氧化物Y,其电极反应为:______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E五种短周期元素,其原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
(1)常温下X、Y的水溶液的pH均为5,则两种水溶液中由水电离出的H+浓度之比是___。
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解。该化合物溶液浓度为0.1 mol/L时, pH最接近_____。
A.5.6 B.7.0 C.8.4 D.13.0
(3)在一个装有可移动活塞的恒温容器中进行如下反应:C2(g)+3A2(g)![]() 2CA3(g) ΔH<0,反应达到平衡后,测得容器中含有C2 0.5mol,A2 0.2mol,CA3 0.2 mol,此时总容积为1.0 L。
2CA3(g) ΔH<0,反应达到平衡后,测得容器中含有C2 0.5mol,A2 0.2mol,CA3 0.2 mol,此时总容积为1.0 L。
①达此平衡前各物质起始的量如下,其中不合理的是_______________;
A.C2 0.6mol, A2 0.5mol, CA3 0mol
B.C2 0mol, A2 0mol, CA3 1.2mol
C.C2 0.55mol,A2 0.35mol,CA3 0.1mol
D.C2 0.8mol,A2 1.1mol,CA3 0mol
②此平衡体系的平衡常数K=____________________;
③如果保持温度和压强不变,向上述平衡体系中加入0.18molC2,平衡将_________(填“正向”、“逆向”或“不”)移动。
(4)已知常温常压下,0.5mol B2A2与足量的D2反应,生成BD2和液态A2D,放出649.8 kJ 的热量。写出B2A2燃烧热的热化学方程式________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是( )
A. 向0.10mol·L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-)
B. 向0.10mol·L-1NaHSO3溶液中通入NH3:c(Na+)>c(NH4+)>c(SO32-)
C. 0.10mol·L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
D. 0.10mol·L-1CH3COONa溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com