
科目: 来源: 题型:
【题目】灼热的焦炭与水蒸气反应所得产物为H2、CO和少量CO2,为了检验产物中的H2和CO(设气体均被充分吸收),设计如下实验装置。下列有关说法错误的是
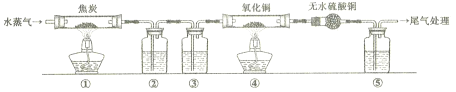
A. 为了实验安全,应先点燃①处酒精灯,后点燃④处酒精灯
B. ②、③、⑤中依次盛装氢氧化钠溶液、浓硫酸和澄清石灰水
C. ④中黑色固体变红色,即可证明产物中一定含有H2和CO中的一种或两种
D. 若用碱石灰替换无水硫酸铜,也可以达到检验H2和CO目的
查看答案和解析>>
科目: 来源: 题型:
【题目】关于化合物![]() (b)、
(b)、![]() (d)、
(d)、![]() (p)的下列说法正确的是
(p)的下列说法正确的是
A. b、d、p都属于芳香烃,且互为同分异构体
B. b、d、p的一氯代物均只有三种
C. b、d、p均可与溴的四氯化碳溶液反应
D. b、d、p中b、d的所有原子可能处于同一平面
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示不同化学元素所组成的化合物,以下说法不正确的是

A. 若图中①为某种多聚体的单体,则①最可能是氨基酸
B. 若②存在于皮下和内脏器官周围等部位,则②是脂肪
C. ③一定是核酸或是组成核酸的单体核苷酸
D. 若④是参与构成植物细胞壁的一种多糖,则④最可能是纤维素
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气是一种常用的化工原料,如合成氨和尿素[CO(NH2)2]等。
(1)以H2合成CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)===2NH3(g)ΔH1=-92.4 kJ·mol-1
②NH3(g)+![]() CO2(g)===
CO2(g)===![]() NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
③NH2CO2NH4(s)===CO(NH2)2(s)+H2O(l)ΔH3=+72.5 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为_______________________________________________________。
(2)电解制H2的原理为C(s)+2H2O(l)![]() CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
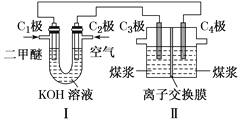
①分别写出电极C1和C3的电极反应式__________________;___________________。
②离子交换膜可能是________(填字母)。
a.阳离子交换膜 b.阴离子交换膜 c.质子交换膜
③已知4.6 g二甲醚参与反应,假设装置Ⅰ的能量转化率为100%,C4极收集到11.2L(标准状况)气体,装置Ⅱ的电流效率η=________。![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】阿伏加德罗常数的值为NA,实验室制备联氨(N2H4)的化学方程式为:2NH3 +NaClO=N2H4 +NaCl+ H2O。下列说法正确的是
A. 0. lmolN2H4中所含质子数为1. 8NA
B. 0. 1mol·L-1的NaClO溶液中,ClO-的数量为0.1NA
C. 消耗4.48LNH3时,转移电子数为0.2NA
D. 1.6g N2H4中存在共价键总数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知几种离子的还原能力强弱顺序为I->Fe2+>Br-,现有200 mL混合溶液中含FeI2、FeBr2各0.10 mol,向其中逐滴滴入氯水(假定Cl2分子只与溶质离子反应,不考虑其他反应)
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是________,剩余Fe2+的物质的量为________。
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为________,若最终所得溶液为400 mL,其中主要阳离子及其物质的量浓度为________。
(3)通过对上述反应的分析,试判断Cl2,I2,Fe3+,Br2四种氧化剂的氧化能力由强到弱的顺序是_________________________________________________。
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式:_________________;上述所有反应共消耗Cl2________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质属于原子晶体的是( )
A. 熔点是1070℃,易溶于水,水溶液能导电
B. 熔点是10.31℃,液态不导电,水溶液能导电
C. 不溶于水,熔点3550℃,不导电
D. 熔点是97.80℃,质软、导电,密度是0.97gcm-3.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com