
科目: 来源: 题型:
【题目】下列有关氯的说法不正确的是( )
A.氯气是由瑞典化学家舍勒首先制得B.氯气是由英国化学家戴维命名的
C.氯元素主要以单质的形式大量存在海水里D.氯气是一种重要的化工原料
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的数值,下列说法不正确的是
A. 标准状况下,1.12L 1H2和0.2g2H2均含有0.1NA个质子
B. 1mol Na2CO3晶体中含有的CO32-数目一定为NA
C. 常温常压下,92g NO2和N2O4的混合气体中含有的原子数为6NA
D. 惰性电极电解饱和食盐水,若电路中通过NA个电子,则阳极产生气体11.2L
查看答案和解析>>
科目: 来源: 题型:
【题目】治疗癌症的有机小分子酯类药物X被批准使用。以芳香族化合物A为主要原料合成X的路线如下:
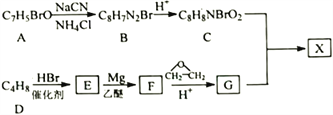
已知:
①核磁共振氢谱显示A有3种化学环境的氢,E只有1种化学环境的氢;
②![]()
③![]()
回答下列问题:
(1)A的名称是______________________;G中官能团名称是____________________。
(2)C在一定条件下反应生成高分子化合物,该反应的化学方程式为:__________________________。
(3)D生成E的反应类型为_____________________。
(4)X的结构简式为_____________________。
(5)已知:同一个碳原子若连有两个—OH时,易转化成![]() 。H是C的同分异构体,写出两种满足下列要求的H的结构简式______________________。
。H是C的同分异构体,写出两种满足下列要求的H的结构简式______________________。
①苯环上有两个取代基;
②能发生银镜反应,且在碱性条件下水解的两种产物也能发生银镜反应。
(6)参照上述合成路线和信息,用乙烯、乙醚、环氧乙烷为原料(其他无机试剂任选)合成1,6-己二酸_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙(CaO2)在室温下稳定,加热至350℃左右,迅速分解。微溶于水,不溶于乙醇,可溶于稀酸生成过氧化氢。实验室用如下方法制备CaO2并测定其纯度。过氧化钙的制备实验装置和步骤如下:
将盛有H2O2溶液和氨水混合液的三颈烧瓶置于冷水浴中,在搅拌下滴入CaCl2溶液,析出固体CaO2·8H2O。对所得固体过滤,用5mL无水乙醇洗涤2![]() 3次,转移至坩埚于烘箱内105℃下脱水干燥,冷却后称重,得产品CaO2。回答下列问题:
3次,转移至坩埚于烘箱内105℃下脱水干燥,冷却后称重,得产品CaO2。回答下列问题:
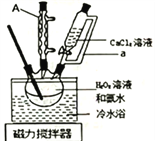
(1)仪器A的名称为:_____________________;恒压分液漏斗的导管a的作用为_________________。
(2)三颈烧瓶中发生反应的化学方程式为___________________________;将三颈烧瓶置于冷水浴中,其主要目的为________________________________。
(3)用无水乙醇代替水洗涤的目的是:___________________________;判断脱水干燥是否完全,需要至少冷却后称重____________次。
(4)过氧化钙纯度的测定,装置如下图所示:
检查装置气密性后,精确称取m g过氧化钙样品加入试管中,调整甲管内液面读数在0-1mL之间,并与乙管的液面相平,记下甲管内液面的初读数V1mL。加热,过氧化钙逐渐分解放出氧气,完全分解,停止加热冷却至室温后,使甲乙两管的液面相平,记下甲管内液面的终读数V2mL,设在此温度和压强下气体摩尔体积为VmL·mol-1,则样品中CaO2的质量分数为___________%。
(5)过氧化钙用于长途运输鱼苗,可能的原因是____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硅、硼、铜、硒的单质及化合物在现代工业生产中有着广泛应用。回答下列问题:
(1)基态Cu+的核外价层电子排布式为_______________;Be、B、Al的第一电离能由大到小的顺序是______________________________。
(2)硒、硅均能与氢元素形成气态氢化物,若“Si-H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se___ Si(填“>”、“<”)。
(3)SeO32-中Se原子的杂化类型为______,与其互为等电子体的一种分子的分子式是______________。
(4)CuSO4和Cu(NO3)2是自然界中重要的铜盐,向CuSO4熔液中加入过量稀氨水,产物的外界离子的空间构型为_________,Cu(NO3)2中的化学键除了σ键外,还存在_______________。
(5)磷化硼(BP)是一种耐磨材料,熔点高,其晶胞结构如图所示。该晶胞中B的堆积方式为___________,己知该晶体的晶胞参数a pm,用NA代表阿伏加德罗常数的值,则该晶体的密度为____ g·cm-3;构成晶体的两种粒子之间的最近距离为__________pm。
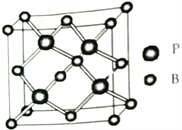
查看答案和解析>>
科目: 来源: 题型:
【题目】向含有NaBr、NaI的溶液中通入过量的Cl2 , 然后将溶液蒸干,并灼烧固体,最后得到的物质是( )
A.NaCl
B.NaCl和NaBr
C.NaCl和NaI
D.NaCl和I2
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
已知:2C(s)+O2(g)=2CO(g) ΔH=- 221 kJ/mol
C(s)+O2(g)=CO2(g) △H=- 393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=![]() ,请写出此反应的热化学方程式:___________________________;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
,请写出此反应的热化学方程式:___________________________;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(S)+2NO(g)![]() N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 15 min | 30 min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~5min内,以CO2表示的该反应速率v(CO2)=______,该条件下的平衡常数K=_______________。
②第15 min后,温度调整到T2,数据变化如上表所示,则T1_______ T2(填“>”、“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应_______移动(填“正向”、“逆向”或“不”);最终达平衡时NO的转化率a=______________。
(3)工业上可以用氨水除去反应C(s)+2NO(g)![]() N2(g)+CO2(g)中产生的CO2,得到NH4HCO3溶液,反应NH4++HCO3-+H2O
N2(g)+CO2(g)中产生的CO2,得到NH4HCO3溶液,反应NH4++HCO3-+H2O![]() NH3·H2O+H2CO3的平衡常数K=________________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5, H2CO3的电离平衡常数Ka1=4×10-7,Ka2=4×10-11)
NH3·H2O+H2CO3的平衡常数K=________________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5, H2CO3的电离平衡常数Ka1=4×10-7,Ka2=4×10-11)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子,下列说法正确的是 ( )
A. X元素原子基态时的电子排布式为[Ar]4s24p3 B. X元素是第四周期第ⅤA族元素
C. Y元素原子的电子排布式为1s22s22p2 D. Z元素具有两性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com