
科目: 来源: 题型:
【题目】三氯异氰尿酸是一种极强的氧化剂和氯化剂,利用氰尿酸(图1)与次氯酸在一定pH下反应可制备三氯异氰尿酸(图2),若原料完全反应生成三氯异氰尿酸,下列说法正确的是
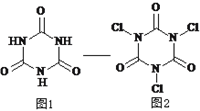
A. 氰尿酸的分子式为C6N3O3H3
B. HClO的电子式为 ![]()
C. 该转化过程有机物发生还原反应
D. 氰尿酸和次氯酸反应的物质的量之比为2 : 3
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)下图中______(填“A”或“B”)是碱式滴定管,进行该实验的第一步操作是____________________。
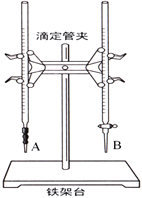
(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直到因加入一滴盐酸后,出现_____________________________(填“现象”)说明达到滴定终点。
(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是(____)
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为________mL。
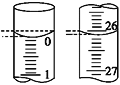
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 0.00 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 |
第三次 | 25.00 | 0.22 | 26.31 |
依据上表数据列式计算该NaOH溶液的物质的量浓度(写出简要过程)。______________
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在三个体积均为2.0L的恒容密闭容器中分别加入一定量的X,发生反应:pX(g) ![]() Y(g)+Z(g),相关数据如下表所示:
Y(g)+Z(g),相关数据如下表所示:
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
X(g) | Y(g) | Z(g) | ||
Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | 0.160 | 0.160 |
Ⅲ | T | 0.20 | 0.090 | 0.090 |
回答下列问题:
(1)若容器Ⅰ中反应经10min达到平衡,则前10min内Y的平均反应速率v(Y)=___________。容器Ⅰ和容器Ⅱ中起始时X的反应速率v(X)Ⅰ___________v(X)Ⅱ(填“大于”“小于”或“等于”)。
(2)已知该正反应为放热反应,则T___________387(填“大于”或“小于”),判断理由是___________。
(3)反应方程式中X的化学计量数p的取值为___________,容器Ⅱ中X的平衡转化率为___________。若起始时向容器Ⅰ中充入0.1molX、0.15molY和0.10molZ,则反应将向___________ (填“正”或“逆”)反应方向进行,判断理由是_____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 标准状况下,向2.24L密闭容器中充满NO2气体,其所含分子数为0.1 NA
B. CuO和Cu2S的混合物80 g中,所含铜粒子数为2NA
C. 常温常压下,22gT2O含中子数为12NA
D. 1.0 L 1.0 mol·L-1的NaNO3水溶液中含有的氧原子数为3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探 究,并共同回答下列问题:
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略).
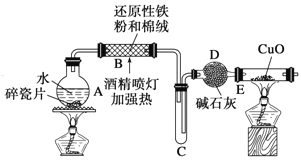
(1)硬质玻璃管 B 中发生反应的化学方程式为:________________________________.。
(2)反应前 A 中投放碎瓷片的目的是___________________.。
(3)装置 E 中的现象是_______________________。
探究二:设计如下实验方案确定反应后硬质玻璃管 B 中黑色固体的成分。
(4)待硬质玻璃管 B 冷却后,取少许其中的固体物质溶于___________________后,将所得溶液分成两份。
(5)一份滴加几滴 KSCN 溶液。若溶液变血红色,推断硬质玻璃管 B 中固体物质的成分为______________________(选 填序号,下同);若溶液未变血红色,推断硬质玻璃管 B 中固体物质的成分为__________________________________。
①一定有 Fe3O4 ②一定有 Fe ③只有 Fe3O4 ④只有 Fe
(6)另一份用_____(填仪器名称)加入_____(填试剂和现象),可以 证明溶液中存在 Fe2+。
探究三:设计如下流程测定反应后硬质玻璃管 B 中固体含铁元素的质量分数。
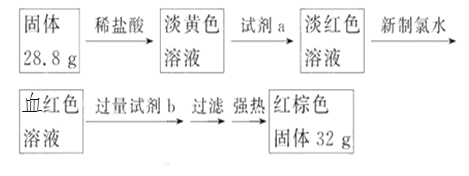
(7)试剂 b 的化学式是_____。
(8)计算反应后 B 装置中铁元素的质量分数为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用酸解法制钛白粉产生的废液生产铁红(Fe2O3)和补血剂乳酸亚铁的生产工业流程如下图所示:
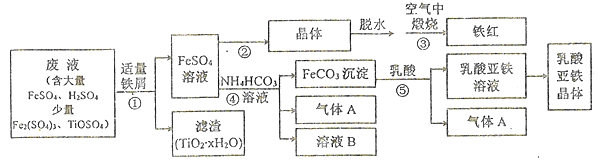
已知;TiOSO4在大量水中加热条件下可完全水解成为TiO2·xH2O沉淀。
请按要求回答下列问题:
(1)步骤①加入适量铁屑的目的是_________。TiOSO4完全水解的化学方程式为_________。
(2)步骤②的系列操作中,需要控制__________、_________条件下,再进行蒸发浓缩、冷却结晶,过滤、洗涤。其中洗涤液选用稀硫酸替代水的优点有__________。
(3)写出步骤③的化学方程式: _________。
(4)某兴趣小组学生以铁屑、稀硫酸、NH4HCO3溶液为原料,欲用下图装置,利用步骤④反应,达到制备FeCO3的目的。
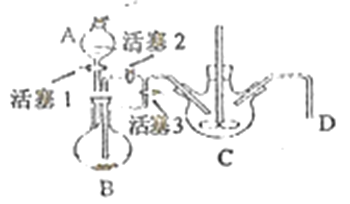
i.NH4HCO3溶液应盛放在装置(填字母) _______中。该装置中涉及的主要反应的离子方程式_________。
ii.达成步骤④反应的操作是__________。
(5)测定步骤②中所得晶体中FeSO4·7H2O的质量分数:
称取ag晶体样品,配成100.00mL溶液,取出25.00mL溶液,用硫酸酸化的0.1000mol/LKMnO4标准溶液滴定(杂质不与KMnO4溶液反应)。平行有效实验滴定消耗KMnO4溶液体积的平均值为20.00mL。则所得晶体中FeSO4·7H2O的质量分数为(设M(FeSO4·7H2O)=bg/mol,用含a、b的表达式表示)_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用漂白粉溶液浸泡过的有色布条,如晾晒在空气中,过一段时间,其漂白效果更好的原因是( )
A.漂白粉被氧化了
B.漂白粉和空气中的二氧化碳充分反应生成了次氯酸
C.有色布条被空气中的氧气氧化
D.漂白粉溶液失去了部分水分,浓度增大了
查看答案和解析>>
科目: 来源: 题型:
【题目】向一定量NaOH溶液的烧杯中通入CO2气体,然后向该溶液中逐滴加入1mol/L盐酸.所加入盐酸溶液的体积与产生二氧化碳气体体积(标准状况)的关系如图所示:
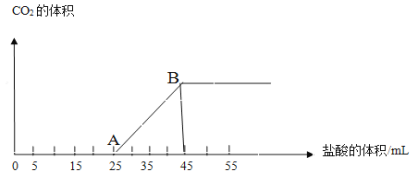
(1)写出OA段所发生反应的离子方程式_____。
(2)当加入35mL盐酸时,所产生的二氧化碳的体积(标准状况)是_____mL。
(3)通入CO2气体后,溶液中所含溶质及溶质的物质的量之比为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物N是制备某药品的中间体,其合成路线如下(部分产物和条件已略):

已知:RCN![]() RCOOH
RCOOH![]() RCOCl
RCOCl![]() RCOOR'
RCOOR'
请按要求回答下列问题:
(1)已知A标准状况下的密度为1.25g/L,则A的结构简式为_______;其分子共平面的原子数目为____________。
(2)B的官能团名称为________。反应①的反应类型为_______。F的名称为_______ 。
(3)P是比A相对分子质量大28的同系物,P的所有可能的结构(含p)数目为______。写出P的属于环烃的同分异构体的结构简式: ______ 。
(4)写出反应②的化学方程式: ______。
(5)已知:  。參照上述流程,设计以G为原料制备K的合成路线(无机试剂任选):_______________。
。參照上述流程,设计以G为原料制备K的合成路线(无机试剂任选):_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com