
科目: 来源: 题型:
【题目】25℃时,向100mL 0.01mol·L-1的NaHA溶液中分别加入浓度均为0.01mol·L-1的NaOH溶液和盐酸,混合溶液的pH随所加溶液体积的变化如图所示(忽略过程中的体积变化)。下列说法不正确的是
A. 25℃时,H2A的第二步电离平衡常数约为10-6
B. 水的电离程度:N>M>P
C. 随着盐酸的不断滴入,最终溶液的pH小于2
D. P点时溶液中存在:2c(H2A)+c(HA-)+c(H+)=c(OH-)+c(Na+)+c(Cl-)
查看答案和解析>>
科目: 来源: 题型:
【题目】微型直接甲醇燃料电池能量密度高,可应用于各类便携式电子产品,其工作原理如图所示。下列说法不正确的是
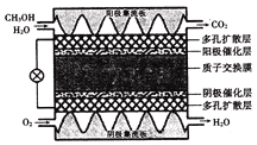
A. 多孔扩散层可起到传导电子的作用
B. 负极上直接通入无水甲醇可提高电池的比能量
C. 当电路中通过3mol e- 时,内电路中有3mol H+ 透过质子交换膜
D. 电池工作时,H+ 向阴极催化层迁移
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A是合成离分子树脂G和合成酚醛树酯的原料之一。相关的合成路线如下图所示:

已知:Ⅰ. (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
Ⅱ.![]()
请回答下列问题:
(1) 经质谱测定,有机物A的相对分子质量为164,燃烧8.2g有机物A,生成标准状况下11.2LCO2和5.4gH2O。则A的分子式是________,A中所含官能团的名称是________。
(2)B的结构简式________。
(3)C的名称是________,请写出在一定条件下C与足量新制氢氧化铜悬浊液反应的化学方程式________。
(4)D-F的反应类型是________,写出由C和苯酚合成酚醛树脂的化学方程式是___________。
(5)有机物![]() 有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式_________。
有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式_________。
Ⅰ.分子中除苯环外,无其它环状结构;
Ⅱ.核磁共振氯谱显示为5组峰;
Ⅲ.能发生水解反应,不能与Na反应
Ⅳ.能发生银镜反应
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中含量位于金属元素的第二位。试回答下列问题:
(1)F元素价层电子排布式为 _______________。
(2)关于B2A2的下列说法中正确的是 _________________。
A. B2A2中的所有原子都满足8电子结构
B. 每个B2A2分子中σ键和π键数目比为1:1
C. B2A2是由极性键和非极性键形成的非极性分子
D. B2A2分子中的B-A键属于s —spσ键
(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是 ___________________。
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因 _____________________________。
(5)A与D可以形成原子个数比分别为2:1,1:1的两种化合物X和Y,其中 Y含有__________键(填“极性键”“非极性键”),A与C组成的两种化合物M和N所含的电子数分别与X、Y相等, N的结构式为__________。
(6)E的氢化物的价层电子对互斥理论模型为 _______,E 原子的杂化方式为 ________杂化。
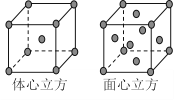
(7)F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为____________,F原子配位数之比为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)制备精细化工产品PbSO4·3PbO·H2O(三盐)的主要流程如下:
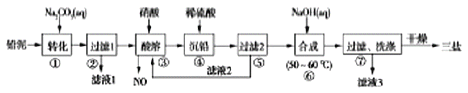
已知:常温下,Ksp(PbSO4)≈1.0×10-8,Ksp(PbSO4)≈1.0×10-13
回答下列问题:
(1)铅蓄电池在生活中有广泛应用,其工作原理是:Pb+PbO+2H2SO4![]() 2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为__________。若铅蓄电池放电前,正、负极质量相等,放若电时转移了lmol电子,则理论上两电极质量之差为_____________。
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为__________。若铅蓄电池放电前,正、负极质量相等,放若电时转移了lmol电子,则理论上两电极质量之差为_____________。
(2)将滤液1、滤液3合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物(Mr=322),其化学式为________________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为________________;滤液2中溶质的主要成分为_____________(写化学式)。
(4)步骤⑥合成三盐的化学方程式为______________。
(5)步骤⑦洗涤的操作是________________________________。
(6)在步骤①的转化中,若硫酸铅和碳酸铅在浊液中共存,则![]() =________。
=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室里欲用KMnO4固体来配制240mL 0.1 molL-1的KMnO4酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、_________
②配制过程中玻璃棒所起的作用是_________
③下列操作对实验结果的影响偏小的是______(填序号)
a.加水定容时俯视刻度线 b.容量瓶内壁附有水珠而未干燥处理
c.若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶
d. 颠倒摇匀后发现凹液面低于刻度线又加水补上
④下列为打乱了的操作示意图,请按先后顺序正确排序_______。

(2)用上述酸性KMnO4溶液来测定FeSO4溶液中Fe2+的物质的量浓度。
①配平该反应的化学方程式:
__FeSO4+ KMnO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O
②该反应中的氧化剂是__________,氧化产物是__________
③若消耗3.16gKMnO4,则该反应转移的电子数目为______
(3)已知反应:①Cl2+2KBr=2KCl+Br2,②2KMnO4+16HCl(浓) =2KCl + 2MnCl2+ 5Cl2↑+8H2O,③Br2+K2S=2KBr+S。
①下列说法正确的是___。
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为KMnO4>Cl2>Br2>S
C.反应②中还原剂与氧化剂的物质的量之比为8:1
D.反应③中1mol还原剂被氧化则转移电子的物质的量为2mol
②用单线桥法标出反应②中电子转移的方向和数目_____。
2KMnO4+16HCl(浓) = 2KCl + 2MnCl2+ 5Cl2↑+8H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】t℃时,卤化银(AgX,X=Cl,Br)的2条溶解平衡曲线如图所示,已知AgCl,AgBr的Ksp依次减小,且p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-),利用pX-pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是
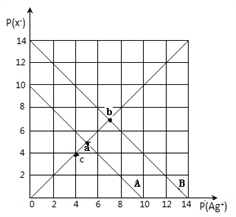
A. t℃时,c点可表示AgCl的不饱和溶液
B. B线表示的是AgBr
C. 取a、b两点处溶液等体积混合,维持t℃不变,混合溶液中一定无白色沉淀生成
D. 在t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K≈104
AgBr(s)+Cl-(aq)平衡常数K≈104
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
![]()
I.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:___________。检验反应后溶液中还存在Fe3+的试剂是__________。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是______,生成1molNa2FeO4转移电子数目为__________。
II.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______,加铁粉后溶液增重的是______;
(2)向Fe2+的溶液中滴加NaOH溶液,现象是___________________。
(3)欲除去FeCl2中FeCl3选用合适的试剂和分离方法,并写出相应离子方程式:__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:①Cl2+2KBr=2KCl+Br2, ②KClO3+6HCl=3Cl2+KCl +3H2O,
③2KBrO3+Cl2=Br2+ 2KClO3,下列说法正确的是
A. 上述三个反应都有单质生成,所以都是置换反应
B. 氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C. 反应②中还原剂与氧化剂的物质的量之比为6:1
D. ③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com